题目内容
15.下列对主要实验现象描述和结论的判断都正确的是( )| 选项 | 实验操作 | 主要现象 | 结论 |
| A | 将在酒精灯灼烧后的铜丝迅速插入无水乙醇中 | 铜丝变黑 | CH3CH2OH发生氧化反应生成CH3COOH,铜丝起催化作用 |
| B | 分别在苯和乙醇中滴加酸性高锰酸钾溶液 | 紫红色都褪去 | 苯和乙醇都有还原性 |
| C | 分别在水、乙醇中 加入钠粒 | 都产生气体 | 产生的气体为氢气 |
| D | 将酒精在空气中点燃 | 产生无色火焰 | 酒精发生氧化反应 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.铜丝变黑可知生成CuO,然后CuO可氧化乙醇生成乙醛;
B.苯与高锰酸钾不反应;
C.水、乙醇均含-OH;
D.酒精燃烧发生淡蓝色的火焰.
解答 解:A.铜丝变黑可知生成CuO,然后CuO可氧化乙醇生成乙醛,又观察到黑色变为红色,且不生成乙酸,故A错误;
B.苯与高锰酸钾不反应,而乙醇能使高锰酸钾褪色,故B错误;
C.水、乙醇均含-OH,均与Na反应生成氢气,故C正确;
D.酒精燃烧发生淡蓝色的火焰,现象不合理,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握有机物的结性质、反应与现象、实验技能为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 全程金卷系列答案
全程金卷系列答案
相关题目
5.下列各组溶液中的各种溶质的物质的量量浓度均为0.1mol•L-1:①H2S ②NaHS ③Na2S ④H2S 和NaHS混合液.下列说法正确的是( )
| A. | 溶液pH值从大到小的是③>②>①>④ | |
| B. | c(H2S) 从大到小是①>④>②>③ | |
| C. | 在H2S 和NaHS混合液中:2c(Na+)═c(H2S)+c(HS-)+c(S2-) | |
| D. | 在NaHS溶液中:c(H+)+c(Na+)═c(OH-)+c(HS-)+c(S2-) |
3. 世某著名学术刊物近期介绍了一种新型中温全瓷铁--空气电池,如图所示.下列有关该电池放电时的说法正确的是( )
世某著名学术刊物近期介绍了一种新型中温全瓷铁--空气电池,如图所示.下列有关该电池放电时的说法正确的是( )
 世某著名学术刊物近期介绍了一种新型中温全瓷铁--空气电池,如图所示.下列有关该电池放电时的说法正确的是( )
世某著名学术刊物近期介绍了一种新型中温全瓷铁--空气电池,如图所示.下列有关该电池放电时的说法正确的是( )| A. | a极发生还原反应 | |
| B. | 正极的电极反应式为FeOx+2xe-═Fe+xO2- | |
| C. | 若有22.4L(标准状况)空气参与反应,则电路中转移4mol电子 | |
| D. | 铁表面发生的反应为xH2O(g)+Fe═FeOx+xH2 |
10.下列实验操作能达到实验目的是( )
| A. | 用向上排空气法收集Na2SO3与浓硫酸反应生成SO2 | |
| B. | 用50mL量筒准确量取25.00mL NaOH溶液 | |
| C. | 除去乙酸乙酯中溶解解的乙酸,加NaOH溶液充分振荡、分液 | |
| D. | 向含有CuCl2的FeC13溶液中加足量铁粉搅拌、过滤,得到纯净FeCl3溶液. |
7.金属钠与下列溶液反应时,既有白色沉淀析出又有气体逸出的是( )
| A. | BaCl2溶液 | B. | K2SO4溶液 | C. | FeCl3溶液 | D. | Ca(HCO3)2溶液 |




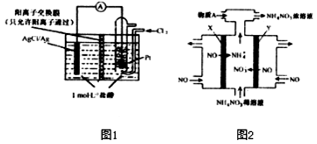 氧化还原反应与生产、生活、科技密切相关,请回答下列问题:
氧化还原反应与生产、生活、科技密切相关,请回答下列问题: