题目内容
14.在如图转化关系中,A为一种金属单质,化合物B为淡黄色粉末.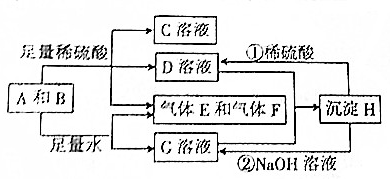
请回答下列问题:
(1)化合物B的化学式为Na2O2.
(2)写出反应①和②的离子方程式;
①Al(OH)3+3H+=Al3++3H2O;②Al(OH)3+OH-=AlO2-+2H2O.
(3)10.8gA单质与足量的NaOH溶液反应,得到的还原产物的质量为1.2g.
分析 根据转化关系D和G两溶液混合得沉淀H,H即能与酸反应又能与碱反应,则H应为Al(OH)3,则G为NaAlO2,D为Al2(SO4)3,化合物B为淡黄色粉末,则B为Na2O2,A为一种金属单质,则A为Al,过氧化钠、铝与酸或水反应得两种气体为氢气、氧气,所以E和F为H2和O2,得溶液C为Na2SO4,据此解答
解答 解:(1)根据上面的分析可知,化合物B的化学式为Na2O2,
故答案为:Na2O2;
(2)反应①的离子方程式为Al(OH)3+3H+=Al3++3H2O,②的离子方程式为Al(OH)3+OH-=AlO2-+2H2O,
故答案为:Al(OH)3+3H+=Al3++3H2O;Al(OH)3+OH-=AlO2-+2H2O;
(3)根据反应2Al+2NaOH+2H2O=2NaAlO2+3H2↑可知,10.8gAl即0.4mol,与足量的NaOH溶液反应,得到的还原产物氢气的物质的量为0.6mol,其质量为0.6×2g=1.2g,
故答案为:1.2.
点评 本题考查无机物推断,涉及钠元素单质化合物性质,以A的颜色及发生的反应为突破口采用正逆结合的方法进行推断,明确物质的性质是解本题关键,题目难度中等.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
15.下列表示正确的是( )
| A. | 含20个电子的氯原子的符号为:3517Cl | |
| B. | 四氯化碳的球棍模型: | |
| C. | 氩的原子结构示意图: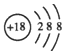 | |
| D. | 乙烯的结构简式:CH2CH2 |
2.以下反应生成的有机物为纯净物的是( )
| A. | CH4和Cl2光照 | B. | 氯乙烯发生加聚反应 | ||
| C. | 正丙醇、异丙醇、浓硫酸共热至170℃ | D. | 甲醇、乙醇、浓硫酸共热至140℃ |
9.用NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A. | 标准状况下,1mol CO2、CO的混合气中含有的碳原子数为NA | |
| B. | 常温常压下,11.2L氯化氢气体中含有的分子数为0.5NA | |
| C. | 1mol氯气与足量的氢氧化钠溶液完全反应转移的电子数为2NA | |
| D. | 1L 1mol•L-1 CuCl2溶液中含有的氯离子数为NA |
19. 如图所示装置中,a、b都是惰性电极,通电一段时间后,b电极附近溶液呈红色.下列说法中正确的是( )
如图所示装置中,a、b都是惰性电极,通电一段时间后,b电极附近溶液呈红色.下列说法中正确的是( )
 如图所示装置中,a、b都是惰性电极,通电一段时间后,b电极附近溶液呈红色.下列说法中正确的是( )
如图所示装置中,a、b都是惰性电极,通电一段时间后,b电极附近溶液呈红色.下列说法中正确的是( )| A. | X是负极,Y是正极 | B. | Cu电极逐渐溶解 | ||
| C. | CuSO4溶液的pH逐渐减小 | D. | CuSO4溶液的pH不变 |
6.下列关于化工生产原理的叙述中,符合当前工业生产实际的是( )
| A. | 氯碱工业中,氢氧化钠在电解槽的阳极区产生 | |
| B. | 硫酸工业中,二氧化硫催化氧化使用催化剂,可增加二氧化硫的转化率 | |
| C. | 合成氨工业中,利用氨易液化,分离出N2、H2循环使用,可提高氨的产率 | |
| D. | 接触法制硫酸中三氧化硫用水吸收制成浓硫酸 |
3.设NA表示阿伏加德罗常数的值,下列说法不正确的是( )
| A. | 100mL0.4mol/L的甲酸中含甲酸的分子数为0.04NA | |
| B. | 在标准状态下,22.4L乙烷与乙烯的混合气体,含碳原子数为2NA | |
| C. | 18g水中含有的电子数为10NA | |
| D. | NA个23Na原子的质量为23g |
4.下列各组反应中,反应物的相对用量对产物组成无影响的是( )
| A. | 铁与稀硝酸 | B. | 硫化氢与氧气 | ||
| C. | 1,3-丁二烯与溴 | D. | 过氧化钠与二氧化碳 |