题目内容
若NA表示阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,NA个任何气体分子的体积都约为22.4L |
| B、在0℃,101kPa时,22.4L氢气中含有NA个氢原子 |
| C、常温常压下,48g O3含有的氧分子数为3NA |
| D、NA个一氧化碳分子和0.5mol甲烷的物质的量之比为1:2 |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A、根据阿伏伽德罗常数计算出气体的物质的量及标况下出气体的体积;
B、根据氢气是双原子分子进行判断;
C、臭氧分子中不含有氧分子;
D、根据一氧化碳的个数计算出物质的量,再进行判断二者物质的量之比.
B、根据氢气是双原子分子进行判断;
C、臭氧分子中不含有氧分子;
D、根据一氧化碳的个数计算出物质的量,再进行判断二者物质的量之比.
解答:
解:A、NA个任何气体分子的物质的量为1mol,标况下气体的体积约为22.4L,故A正确;
B、标况下,22.4L氢气的物质的量为1mol,含有2mol氢原子,含有2NA个氢原子,故B错误;
C、48g臭氧的物质的量为1mol,臭氧中不含有氧气分子,故C错误;
D、一氧化碳的物质的量为1mol,NA个一氧化碳分子和0.5mol甲烷的物质的量之比为2:1,故D错误;
故选:A.
B、标况下,22.4L氢气的物质的量为1mol,含有2mol氢原子,含有2NA个氢原子,故B错误;
C、48g臭氧的物质的量为1mol,臭氧中不含有氧气分子,故C错误;
D、一氧化碳的物质的量为1mol,NA个一氧化碳分子和0.5mol甲烷的物质的量之比为2:1,故D错误;
故选:A.
点评:本题考查了阿伏伽德罗常数,注意标准状况下条件及物质的状态,本题难度不大.

练习册系列答案
相关题目
亚硝酸(HNO2)既可以做氧化剂又可作还原剂,当它在反应中作氧化剂时,可能生成的物质是( )
| A、N2 |
| B、N2O3 |
| C、HNO3 |
| D、NO2 |
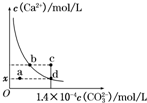 室温时,CaCO3在水中的溶解平衡曲线如图所示,已知:25℃其溶度积为2.8×10-9 mol2/L2,下列说法不正确的是( )
室温时,CaCO3在水中的溶解平衡曲线如图所示,已知:25℃其溶度积为2.8×10-9 mol2/L2,下列说法不正确的是( )| A、x数值为2×10-5 |
| B、c点时有碳酸钙沉淀生成 |
| C、加入蒸馏水可使溶液由d点变到a点 |
| D、b点与d点对应的溶度积相等 |
R为某元素.已知a个RO2的质量为m g,则b g R2H4的物质的量为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
下列关于阿伏加德罗常数NA的说法正确的是( )
| A、1mol/L的NaCl溶液中Na+为NA个 |
| B、1mol水中H原子为2NA个 |
| C、1mol N2H4分子中N和H原子都为NA个 |
| D、2g H2中含NA个电子 |
下列叙述中正确的是( )
| A、CO2是酸性氧化物 |
| B、由一种元素组成的物质一定是单质 |
| C、单质只能用置换反应制取 |
| D、含氧元素的化合物称为氧化物 |
欲配制480mL 0.1mol/L的CuSO4溶液,现选取500mL容量瓶,以下操作正确的是( )
| A、称取8.00 g硫酸铜,配成500 mL溶液 |
| B、称取7.68 g硫酸铜,加入500 mL水 |
| C、称取12.0 g胆矾,配成480 mL溶液 |
| D、称取12.5 g胆矾,配成480 mL溶液 |
 甲醇是一种可再生能源,具有广泛的开发和应用前景.
甲醇是一种可再生能源,具有广泛的开发和应用前景. 将35.8gNa2CO3和NaHCO3的固体混合物溶于足量水中,向其中逐滴加入1mol?L-1的盐酸至不再产生气体为止,测得共产生CO28.96L(标准状况)(气体溶解忽略不计).回答:
将35.8gNa2CO3和NaHCO3的固体混合物溶于足量水中,向其中逐滴加入1mol?L-1的盐酸至不再产生气体为止,测得共产生CO28.96L(标准状况)(气体溶解忽略不计).回答: