��Ŀ����
7��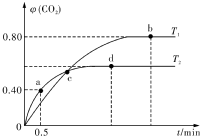 ����I2O5����CO��Ⱦ�ķ�ӦΪ��5CO��g��+I2O5��s���T5CO2��g��+I2��s������ͬ�¶��£���װ������I2O5�����2L�����ܱ�������ͨ��4molCO�����CO2�����������ʱ��t�仯������ͼ����ش�
����I2O5����CO��Ⱦ�ķ�ӦΪ��5CO��g��+I2O5��s���T5CO2��g��+I2��s������ͬ�¶��£���װ������I2O5�����2L�����ܱ�������ͨ��4molCO�����CO2�����������ʱ��t�仯������ͼ����ش���1��T2ʱ��0��0.5min�ڵķ�Ӧ����v��CO��=1.6mol•L-1•min-1��
��2��T1ʱ��ѧƽ�ⳣ��K=1024��
��3������˵������ȷ����BD������ĸ��ţ���
A�������������ܶȲ��䣬������Ӧ�ﵽƽ��״̬
B�������¶��£�C��ʱ��ϵ�л�������ѹǿ���
C��d��ʱ��������ϵѹǿ��CO��ת���ʲ���
D��b���d��ʱ��ѧƽ�ⳣ���Ĵ�С��ϵ��Kb��Kd��
���� ��1��������ʼ����a��ʱCO2�����������������������������ʽ���㼴������ӷ�Ӧ��ʼ��a��ʱ�ķ�Ӧ����Ϊv��CO����
��2������b��ʱCO2����������գ�CO2�����CO��CO2��ƽ��Ũ�Ƚ������T1ʱ��ѧƽ�ⳣ��K��
��3��A����Ϊ����Ϊ���ݣ�����Ӧǰ�����������仯�����������������ܶ��DZ�����������ʱ������Ӧ�ﵽƽ��״̬��
B��c��Ϊ���㣬���������ʵ����ֱ���ȣ�
C����Ӧǰ������������䣬ѹǿ�仯��ƽ����Ӱ�죻
D��b���d��ʱ������CO2���������˵�����еij̶ȴ���ѧƽ�ⳣ����Kb��Kd��
��� �⣺��1��a��ʱ��5CO��g��+I2O5��s��?5CO2��g��+I2��s��
��ʼ��/mol 4 0
ת����/mol x x
a����/mol 4-x x
����a��ʱCO2����������գ�CO2��=$\frac{x}{4}$=0.40����x=1.6mol
��ӷ�Ӧ��ʼ��a��ʱ�ķ�Ӧ����Ϊv��CO��=$\frac{1.6mol}{2L��0.5min}$=1.6mol•L-1•min-1��
�ʴ�Ϊ��1.6mol•L-1•min-1��
��2��T1ʱ��5CO��g��+I2O5��s��?5CO2��g��+I2��s��
��ʼ��/mol 4 0
ת����/mol y y
b����/mol 4-y y
����b��ʱCO2����������գ�CO2��=$\frac{y}{4}$=0.80����y=3.2mol��c��CO��=0.4mol•L-1��c��CO2��=1.6mol•L-1
T1ʱ��ѧƽ�ⳣ��K=$\frac{c��CO{\;}_{2}��{\;}^{5}}{c��CO��{\;}^{5}}$=$\frac{1.6{\;}^{5}}{0��{4}^{5}}$=1024��
�ʴ�Ϊ��1024��
��3��A����Ϊ����Ϊ���ݣ�����Ӧǰ�����������仯�����������������ܶȲ���ʱ��������Ӧ�ﵽƽ��״̬����A��ȷ��
B��c��Ϊ���㣬�������ʵ����ֱ���ȣ����������¶��£���ϵ�л�������ѹǿ���ȣ���B����
C����Ӧǰ������������䣬ѹǿ�仯��ƽ����Ӱ�죬CO��ת���ʲ��䣬��C��ȷ��
d��b���d��ʱ������CO2���������˵�����еij̶ȴ���ѧƽ�ⳣ����Kb��Kd����D����
�ʴ�Ϊ��BD��
���� �����ۺϿ��黯ѧ��Ӧ���ʺͻ�ѧƽ�ⳣ������ؼ��㡢��ѧƽ���ƶ�ԭ����Ϊ�߿��������ͣ�������ѧ���ķ��������ͼ��������Ŀ��飬�ۺ��Ժ�ǿ���ѶȽϴ�ע����ջ�ѧƽ�ⳣ���ļ����Լ�ƽ���ƶ���Ӱ�죮

 ��У����ϵ�д�
��У����ϵ�д�
 ��
��
 ��6Fe2����14H
��6Fe2����14H ��=2Cr3����6Fe3����7H2O��
��=2Cr3����6Fe3����7H2O�� ��NO
��NO
 ��Cl����S2��
��Cl����S2��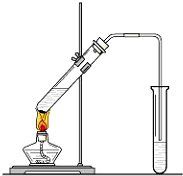 ��ʵ�������ǿ�������ͼ��ʾ��װ������ȡ�����������Իش��������⣺
��ʵ�������ǿ�������ͼ��ʾ��װ������ȡ�����������Իش��������⣺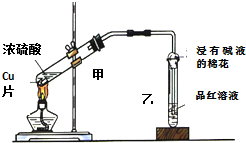 ����ͼװ����Ũ�����ͭ��Ӧ��ʵ�飬ʵ������й۲쵽���Թܵײ���һЩ��ɫ���壬���Թ���Ʒ����Һ��ɫ��
����ͼװ����Ũ�����ͭ��Ӧ��ʵ�飬ʵ������й۲쵽���Թܵײ���һЩ��ɫ���壬���Թ���Ʒ����Һ��ɫ��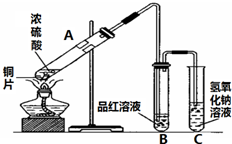 ͼ�ǽ���ͭ��Ũ���ᷴӦ�����в�������װ�ã�
ͼ�ǽ���ͭ��Ũ���ᷴӦ�����в�������װ�ã�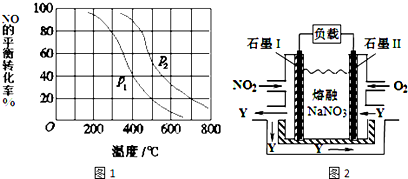
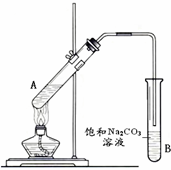 �����dzµ��㡱��������Ϊ���ڴ������������������ζ��������������ʵ��������Ҳ��������ͼ��ʾ��װ����ȡ�����������ش��������⣺
�����dzµ��㡱��������Ϊ���ڴ������������������ζ��������������ʵ��������Ҳ��������ͼ��ʾ��װ����ȡ�����������ش��������⣺