题目内容
把1120mL标准状况时的体积氯化氢溶解于水,配制成500mL溶液,该溶液的氢离子浓度为 mol/L,溶液的pH值为 .
考点:物质的量浓度的相关计算,pH的简单计算
专题:计算题
分析:带入n=
氯化氢的物质的量,然后带入c=
求算浓度,根据氢离子的浓度带入PH=-lgc(H+)求算PH.
| V |
| Vm |
| n |
| V |
解答:
解:n(HCl)=
=0.05mol,c(HCl)=
=0.1mol/L;
c(H+)=c(HCl)=0.1 mol/L,PH=-lgc(H+)=-lg0.1=1,
故答案为:0.1;1.
| 1.12L |
| 22.4L/mol |
| 0.05mol |
| 0.5L |
c(H+)=c(HCl)=0.1 mol/L,PH=-lgc(H+)=-lg0.1=1,
故答案为:0.1;1.
点评:本题考查了物质的量为中心的计算、PH的计算,难度不大,注意基本公式的联合应用.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
有关
C的说法正确的是( )
13 6 |
| A、电子数为13 |
| B、质子数为6 |
| C、中子数为6 |
| D、质量数为6 |
下列说法错误的是( )
| A、CO2和漂白粉作用,可生成具有氧化性的物质 |
| B、SiO2与烧碱溶液反应后,溶液的碱性一定减弱 |
| C、SO2通入氢硫酸溶液中,溶液的酸性一定减弱 |
| D、NO2分子在一定条件下可以相互结合为N2O4分子 |
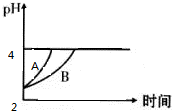 化学学科中存在以下四种平衡体系:化学平衡、电离平衡、水解平衡和溶解平衡,且均符合勒夏特列原理.请回答下列问题:
化学学科中存在以下四种平衡体系:化学平衡、电离平衡、水解平衡和溶解平衡,且均符合勒夏特列原理.请回答下列问题: )在催化剂作用下发生缩聚反应生成聚乳酸:
)在催化剂作用下发生缩聚反应生成聚乳酸: