题目内容
20. 如图所示装置,电流表G发生偏转,a极逐渐变粗,同时b极逐渐变细,c为电解质溶液,则a、b、c应是下列各组中的( )
如图所示装置,电流表G发生偏转,a极逐渐变粗,同时b极逐渐变细,c为电解质溶液,则a、b、c应是下列各组中的( )| A. | a是Ag、b是Fe、c为AgNO3溶液 | B. | a是Fe、b是Ag、c为AgNO3溶液 | ||
| C. | a是Zn、b是Cu、c为稀H2SO4 | D. | a是Cu、b是Zn、c为稀H2SO4 |
分析 原电池中负极的活泼性大于正极的活泼性,负极上金属失电子变成离子进入溶液,质量减少,正极上得电子发生还原反应,正极上析出物质,若析出的物质是金属,则正极质量增加,据此分析.
解答 解:该原电池中,a极逐渐变粗,同时b极逐渐变细,所以b作负极,a作正极,b的活泼性大于a的活泼性,所以排除BC选项;
a极逐渐变粗,说明有金属析出,D选项析出氢气不是金属,A选项析出金属,所以A符合题意.
故选A.
点评 本题考查了原电池原理,难度不大,明确正负极的判断方法,注意不能仅根据金属的活泼性判断正负极,要根据发生反应的反应类型判断正负极,如:Mg、Al、NaOH溶液构成的原电池,铝作负极,镁作正极.

练习册系列答案
相关题目
17.为加快化学反应速率采取的措施是( )
| A. | 食物放在冰箱中 | B. | 在月饼包装内放脱氧剂 | ||
| C. | 燃煤发电时用煤粉代替煤块 | D. | 橡胶制品中添加抑制剂 |
11. 异鼠李素的结构简式如图所示.当与等量该有机物反应时,最多消耗Br2、Na、NaOH的物质的量之比为( )
异鼠李素的结构简式如图所示.当与等量该有机物反应时,最多消耗Br2、Na、NaOH的物质的量之比为( )
 异鼠李素的结构简式如图所示.当与等量该有机物反应时,最多消耗Br2、Na、NaOH的物质的量之比为( )
异鼠李素的结构简式如图所示.当与等量该有机物反应时,最多消耗Br2、Na、NaOH的物质的量之比为( )| A. | 1:1:1 | B. | 4:4:3 | C. | 5:4:3 | D. | 3:5:1 |
15.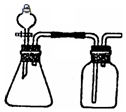 利用下列各组物质能制备和收集相应的气体,且可采用如图所示装置(图中尾气处理装置略)的是( )
利用下列各组物质能制备和收集相应的气体,且可采用如图所示装置(图中尾气处理装置略)的是( )
①亚硫酸钠和浓硫酸
②铝和烧碱溶液
③铜和稀硝酸
④铜和浓硫酸
⑤双氧水(H2O2)和二氧化锰
⑥铜和浓硝酸.
 利用下列各组物质能制备和收集相应的气体,且可采用如图所示装置(图中尾气处理装置略)的是( )
利用下列各组物质能制备和收集相应的气体,且可采用如图所示装置(图中尾气处理装置略)的是( )①亚硫酸钠和浓硫酸
②铝和烧碱溶液
③铜和稀硝酸
④铜和浓硫酸
⑤双氧水(H2O2)和二氧化锰
⑥铜和浓硝酸.
| A. | ①⑤⑥ | B. | ①③⑥ | C. | ①②⑤ | D. | ③⑤⑥ |
12.在一定温度下,将2molSO2和1molO2充入一固定容积的密闭容器中,在催化剂作用下发生如下放热反应:2SO2(g)+O2(g)?2SO3(g),对该反应的下列说法中正确的是( )
| A. | 若向该体系中通入过量的二氧化硫,则氧气的转化率可达到100% | |
| B. | 该反应过程中SO2和O2的总能量一定低于SO3的总能量 | |
| C. | 当达到化学平衡时,该容器中SO2和SO3共2mol | |
| D. | 当达到反应限度时,单位时间内生成nmolO2,同时消耗2n molSO3 |
7.下列气体不能用排水法收集的是( )
| A. | NO | B. | NO2 | C. | O2 | D. | CO |
 (1)氨气易溶于水生成氨水,氨水电离生成铵根离子,铵根离子中氮原子采取sp3杂化,NH4+中HNH键角比NH3中HNH键角大,原因是氨气分子中氮原子上有一对孤对电子,铵根离子中氮原子上没有孤对电子,排斥力小.
(1)氨气易溶于水生成氨水,氨水电离生成铵根离子,铵根离子中氮原子采取sp3杂化,NH4+中HNH键角比NH3中HNH键角大,原因是氨气分子中氮原子上有一对孤对电子,铵根离子中氮原子上没有孤对电子,排斥力小.