题目内容
下列反应的离子方程式正确的是( )
A.足量的溴化亚铁和少量的氯气反应:2Fe2++Cl2=2Fe3++2Cl-
B.亚硫酸氢铵和氢氧化钠的反应: +OH-
+OH-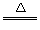 NH3↑+H2O
NH3↑+H2O
C.二氧化硫气体通入过量的Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO
D.Ca(HCO3)2溶液与少量NaOH溶液反应:
A
【解析】还原性Fe2+>Br-,氯气不足时,氯气先氧化Fe2+,A正确;亚硫酸氢铵和氢氧化钠反应时,优先进行反应 ,NaOH过量时再发生反应:NH4++OH-
,NaOH过量时再发生反应:NH4++OH- NH3↑+H2O,B错;HClO具有强氧化性,能氧化CaSO3,C错;NaOH溶液少量时的离子方程式是:Ca2++
NH3↑+H2O,B错;HClO具有强氧化性,能氧化CaSO3,C错;NaOH溶液少量时的离子方程式是:Ca2++ +OH-=CaCO3↓+H2O,D错
+OH-=CaCO3↓+H2O,D错

练习册系列答案
相关题目
如图是某硫酸试剂瓶标签上的部分文字。据此,下列说法正确的是( )
硫酸 化学纯(CP)(500 mL) 品名:硫酸 化学式:H2SO4 相对分子质量:98 密度:1.84 g/cm3 质量分数:98% |
A.该硫酸的物质的量浓度为9.2 mol/L
B.1 mol Zn与足量的该硫酸反应生成2 g氢气
C.该硫酸与等体积水混合所得溶液的物质的量浓度等于9.2 mol/L
D.向50 mL该硫酸溶液中加入足量的铜片,加热充分反应后,被还原的硫酸的物质的量小于0.46 mol







