题目内容
14.下列属于电解质的是( )| A. | KCl晶体 | B. | NaCl溶液 | C. | 金属铜 | D. | CO2 |
分析 电解质:在水溶液中或熔融状态下能导电的化合物;例:酸、碱、盐,金属氧化物等;
非电解质:在水溶液中和熔融状态下不能导电的化合物;例:有机物,非金属氧化物;
电解质与非电解质都是化合物,据此分析解答.
解答 解:A.氯化钾为化合物,在水溶液中或熔融状态下能导电,属于电解质,故A正确;
B.氯化钠溶液是混合物,不是电解质,故B错误;
C.金属铜为单质,不是电解质,故C错误;
D.二氧化碳在水溶液中和熔融状态下本身都不能电离出自由离子,属于非电解质,故D错误;
故选:A.
点评 本题考查了电解质的判断,难度不大,注意电解质和非电解质都必须是化合物,单质和混合物既不是电解质也不是非电解质.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
5.如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22.下列说法正确的是( )
| X | Y | ||
| W | Z | ||
| T |
| A. | 原子半径的大小顺序为:rZ>rW>rY>rX | |
| B. | 离子Y2-和X3-的核外电子数和电子层数都不相同 | |
| C. | 物质WY2、WZ4均有熔点高、硬度大的特性 | |
| D. | T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 |
2.能源、环境与人类生活密切相关,研究它们的综合利用有重要意义.
Ⅰ.二甲醚可代替汽油作新型清洁燃料.常温常压下,二氧化碳加氢可选择性生产二甲醚(CH3OCH3)或一氧化碳.已知二甲醚、氢气的燃烧热分别为-1455kJ/mol,-285.8kJ/mol
(1)写出CO2加氢转化为CH3OCH3(g)和H2O(l)的热化学方程式2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(l)△H=-259.8kJ•mol-1,该反应的平衡常数的表达式为)
$\frac{c(C{H}_{3}OC{H}_{3})}{{c}^{2}(C{O}_{2}){c}^{6}({H}_{2})}$..
(2)等物质的量的CO和H2在一定条件下可合成CH3OCH3,同时还产生了一种可参与大气循环的无机化合物,该反应的化学方程式为:3CO+3H2═CH3OCH3+CO2.
(3)二甲醚燃料电池原理如图1所示
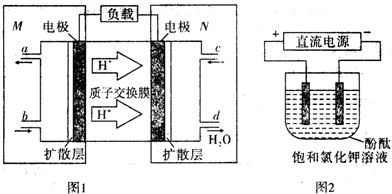
①M区发生的电极反应式为CH3OCH3+3H2O-12e-=2CO2+12H+.
②用上述电池做电源,用图2装置电解饱和氯化钾溶液(电极均为惰性电极),设饱和氯化钾溶液体积为500mL,当溶液的pH值变为13时(在常温下测定),若该燃料电池的能量利用率为80%,则需消耗CH3OCH3的质量为0.24g(假设溶液电解前后体积不变,保留2位有效数字).
Ⅱ.硝化法是一种古老的生产硫酸的方法,同时实现了氮氧化物的循环转化,主要反应为:NO2(g)+SO2(g)?SO3(g)+NO(g)△H=-41.8kJ•mol-1
(1)下列说法中可以说明该反应已达到平衡状态的是bd
a.体系内混合气体的密度保持不变 h.v(NO2)正=v(SO3)逆
c.容器内气体的总压强保持不变 d.NO体积分数不再改变
(2)某温度下,NO2(g)+SO2(g)?SO3(g)+NO(g)的平衡常数K=$\frac{9}{4}$,该温度下在甲、乙、丙三个体积为2L的恒容密闭容器中,投入NO2(g)和SO2(g),其起始浓度如表所示,
①10min后,甲中达到平衡,则甲中反应的平均速率v(NO2)=0.006mol/(L•min).
②丙达到平衡所用的时间<10min(填“<”“>”“=”),达到平衡后,设甲、乙、丙中SO2(g)的转化率分别为a、b、c,则三者的大小关系为a=c<b.
Ⅰ.二甲醚可代替汽油作新型清洁燃料.常温常压下,二氧化碳加氢可选择性生产二甲醚(CH3OCH3)或一氧化碳.已知二甲醚、氢气的燃烧热分别为-1455kJ/mol,-285.8kJ/mol
(1)写出CO2加氢转化为CH3OCH3(g)和H2O(l)的热化学方程式2CO2(g)+6H2(g)=CH3OCH3(g)+3H2O(l)△H=-259.8kJ•mol-1,该反应的平衡常数的表达式为)
$\frac{c(C{H}_{3}OC{H}_{3})}{{c}^{2}(C{O}_{2}){c}^{6}({H}_{2})}$..
(2)等物质的量的CO和H2在一定条件下可合成CH3OCH3,同时还产生了一种可参与大气循环的无机化合物,该反应的化学方程式为:3CO+3H2═CH3OCH3+CO2.
(3)二甲醚燃料电池原理如图1所示

①M区发生的电极反应式为CH3OCH3+3H2O-12e-=2CO2+12H+.
②用上述电池做电源,用图2装置电解饱和氯化钾溶液(电极均为惰性电极),设饱和氯化钾溶液体积为500mL,当溶液的pH值变为13时(在常温下测定),若该燃料电池的能量利用率为80%,则需消耗CH3OCH3的质量为0.24g(假设溶液电解前后体积不变,保留2位有效数字).
Ⅱ.硝化法是一种古老的生产硫酸的方法,同时实现了氮氧化物的循环转化,主要反应为:NO2(g)+SO2(g)?SO3(g)+NO(g)△H=-41.8kJ•mol-1
(1)下列说法中可以说明该反应已达到平衡状态的是bd
a.体系内混合气体的密度保持不变 h.v(NO2)正=v(SO3)逆
c.容器内气体的总压强保持不变 d.NO体积分数不再改变
(2)某温度下,NO2(g)+SO2(g)?SO3(g)+NO(g)的平衡常数K=$\frac{9}{4}$,该温度下在甲、乙、丙三个体积为2L的恒容密闭容器中,投入NO2(g)和SO2(g),其起始浓度如表所示,
| 起始浓度 | 甲 | 乙 | 丙 |
| c(NO2)/mol•L-1 | 0.10 | 0.20 | 0.20 |
| c(SO2)/mol•L-1 | 0.10 | 0.10 | 0.20 |
②丙达到平衡所用的时间<10min(填“<”“>”“=”),达到平衡后,设甲、乙、丙中SO2(g)的转化率分别为a、b、c,则三者的大小关系为a=c<b.
9.下列各组离子能在溶液中大量共存的是( )
| A. | K+、Na+、NO3-、SO42- | B. | Al3+、OH-、Cl-、Na+ | ||
| C. | NO3-、Cl-、Na+、Ag+ | D. | CO32-、H+、Ca2+、Na+ |
19.在酸性溶液中,下列各组离子可能共存的是( )
| A. | NH4+、NO3-、CO32-、Na+ | B. | Na+、Ba2+、NO3-、HCO3- | ||
| C. | SO42-、Fe3+、K+、Cl- | D. | NO3-、K+、SO32-、Mg2+ |
6.下列说法正确的是( )
| A. | 非自发反应在任何条件下都不能发生 | |
| B. | 冰融化为水的过程中△H<0,△S>0 | |
| C. | 2H2(g)+02(g)=2H2O(l)△H=-572kJ•mol-1此反应在低温时可以自发进行 | |
| D. | 知道了某过程有自发性之后,可预测过程发生完成的快慢 |
3.设NA为阿伏伽德罗常数的值.下列说法正确的是( )
| A. | 80mL10mol/L的浓盐酸与足量的MnO2加热反应,产生Cl2分子数约为0.2NA | |
| B. | 一定条件下,将1molN2和3molH2混合,充分反应后转移电子数为6NA | |
| C. | 钠在空气中燃烧可生成多种氧化物.23g钠充分燃烧时转移电子数为1NA | |
| D. | 常温常压下,等质量的CO和N2中含有原子数目均为2NA |
7.关于下列各图的叙述正确的是( )

| A. | 甲中△H1=-(△H2+△H3) | |
| B. | 乙表示恒温恒容条件下发生的可逆反应2NO2(g)═N2O4(g)中,各物质的浓度与其消耗速率之间的关系,其中交点A对应的状态为化学平衡状态 | |
| C. | 丙表示A、B两物质的溶解度随温度变化情况,将tl℃时A、B的饱和溶液分别升温至t2℃时,溶质的质量分数B>A | |
| D. | 丁表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH大于等物质的量浓度的NaB溶液的pH |