题目内容
对于N2(g)+3H2(g)?2NH3(g),不能作为反应达到平衡状态的判断依据是( )
| A、N2、H2、NH3的浓度不再发生变化 |
| B、恒容密闭容器中总压强不变 |
| C、生成氨气的速率与氨气分解的速率相等 |
| D、单位时间内生成1molN2,同时生成3molH2 |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:化学反应达到平衡状态时,正逆反应速率相等,各物质的浓度不再发生变化,由此衍生的一些物理量不再变化,注意反应化学方程式中气体的化学计量数之和前后不等的特点,以此判断.
解答:
解:A.当该反应达到平衡状态时,各物质的浓度不再发生变化,则各种物质的质量分数不再变化,可以说明达到平衡状态,故A不选;
B.该反应反应前后气体体积不同,反应达到平衡状态时气体的压强不再变化,故B不选;
C.生成氨气的速率和分解氨气的速率相等,则氨气的正逆反应速率相等,所以可以说明达到平衡状态,故C不选;
D.单位时间里每增加1 mol N2,同时生成3 molH2,都是指逆反应,所以不能反应说明达到平衡状态,故D选;
故选:D.
B.该反应反应前后气体体积不同,反应达到平衡状态时气体的压强不再变化,故B不选;
C.生成氨气的速率和分解氨气的速率相等,则氨气的正逆反应速率相等,所以可以说明达到平衡状态,故C不选;
D.单位时间里每增加1 mol N2,同时生成3 molH2,都是指逆反应,所以不能反应说明达到平衡状态,故D选;
故选:D.
点评:本题考查化学平衡状态的判断,题目难度不大,注意方程式中气体的化学计量数关系,注意平衡时的浓度关系、物质的量关系不能作为判断是否平衡的依据.

练习册系列答案
 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案
相关题目
用漂白粉溶液浸泡过的有色布条,如晾晒在空气中,过一段时间,其漂白效果更好的原因是( )
| A、有色布条被空气中的氧气氧化 |
| B、漂白粉溶液失去了部分水分,浓度增大了 |
| C、漂白粉和空气中的二氧化碳充分反应生成了次氯酸 |
| D、漂白粉被氧化了 |
下列说法正确的是( )
| A、分子式相同而结构不同的有机物一定互为同分异构体 |
| B、具有同一通式、分子组成上相差若干个CH2原子团的物质一定属于同系物 |
| C、组成元素相同、结构不同的有机物都互为同分异构体 |
| D、只要相对分子质量相同就一定属于同分异构体 |
下列装置中能构成原电池的是( )
A、 |
B、 |
C、 |
D、 |
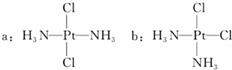 科学家发现铂的两种化合物a和b(见图),实验测得a和b具有不同的性质,且a具有抗癌作用,而b没有.下列关于a、b的叙述错误的是( )
科学家发现铂的两种化合物a和b(见图),实验测得a和b具有不同的性质,且a具有抗癌作用,而b没有.下列关于a、b的叙述错误的是( )| A、a和b互为同分异构体 |
| B、a和b互为“镜”和“像”的关系 |
| C、a和b的空间构型是平面四边形 |
| D、a和b分别是非极性分子和极性分子 |
下列说法正确的是( )
| A、1 mol物质的质量就是该物质的摩尔质量 |
| B、1 mol气体的体积就是气体摩尔体积 |
| C、1 mol任何粒子的相应粒子数叫做阿伏加德罗常数 |
| D、1 mol HCl溶于1 L水中,所得盐酸的物质的量浓度为1 mol?L-1 |
有关金属的腐蚀与防护的叙述正确的是( )
| A、金属的化学腐蚀比电化学腐蚀普遍 |
B、 如图装置的原理是“牺牲阳极的阴极保护法” |
| C、金属腐蚀的本质是M-ne-→M n+而被损耗 |
| D、用铝质铆钉来接铁板,铁板易被腐蚀 |
下列说法正确的是( )
| A、采用天然石材装修家居,可减轻室内甲醛等有机物和放射性物质的污染 |
| B、所有烷烃和蛋白质分子中都存在碳碳单键 |
| C、回收电子垃圾通过高温焚烧熔出金属,可实现资源循环利用和绿色环保 |
| D、乙醇可以转化成乙酸,乙醇和乙酸都能发生取代反应 |
SO2的回收利用方案如图所示.下列说法错误的是( )
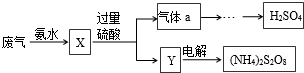

| A、X可能含有2种盐 |
| B、a是SO3 |
| C、Y中含NH4HSO4 |
| D、(NH4)2S2O8中S的化合价不可能为+7 |