题目内容
【题目】下图是第3周期11~17号元素某些性质变化趋势的柱形图。下列有关说法中正确的是( )
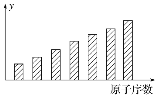
A.y轴表示的可能是电离能B.y轴表示的可能是电负性
C.y轴表示的可能是原子半径D.y轴表示的可能是形成基态离子转移的电子数
【答案】B
【解析】
A. 对于第3周期11~17号元素,随着原子序数的增大,第一电离能总体上呈增大趋势,但Mg、P特殊,Mg的3s电子全满为稳定结构,P的3p电子半满为稳定结构,则第一电离能大于相邻的元素,即第一电离能不是随着原子序数的递增而增大,A错误;
B. 同周期随原子序数的增大,元素的非金属性增强,则元素的电负性增强,B正确;
C. 同周期随原子序数的增大,原子半径减小,与图像不符,C错误;
D. 形成基态离子转移的电子数依次为Na为1,Mg为2,Al为3,Si不易形成离子,P为3,S为2,Cl为1,与图像不符,D错误;
答案选B。

练习册系列答案
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案
相关题目




