题目内容
下列有关阿伏加德罗常数(NA)的说法错误的是( )
| A、标准状况下,18克水含有10NA个质子. |
| B、常温常压下,16gO2和O3的混合物中,约含6.02×1023个氧原子 |
| C、0.1molOH-含有NA个电子 |
| D、5.6g金属铁和足量盐酸反应,失去的电子数目为0.3NA |
考点:阿伏加德罗常数
专题:阿伏加德罗常数和阿伏加德罗定律
分析:A.气体摩尔体积适用对象为气体;
B.根据氧气和臭氧中含有的氧原子的质量计算出氧原子的物质的量及数目;
C.1个氢氧根离子含有10个电子;
D.铁与盐酸反应生成二价铁离子.
B.根据氧气和臭氧中含有的氧原子的质量计算出氧原子的物质的量及数目;
C.1个氢氧根离子含有10个电子;
D.铁与盐酸反应生成二价铁离子.
解答:
解:A.标况下,水为液态,不能使用气体摩尔体积,故A错误;
B.16g氧气和臭氧中含有16g氧原子,含有1mol氧原子,约含6.02×1023个氧原子,故B正确;
C.1个氢氧根离子含有10个电子,0.1molOH-含有0.1mol×10×NA=NA个电子,故C正确;
D.5.6g金属铁物质的量为0.1mol,和足量盐酸反应,失去的电子数目为0.2NA,故D错误;
故选:BC.
B.16g氧气和臭氧中含有16g氧原子,含有1mol氧原子,约含6.02×1023个氧原子,故B正确;
C.1个氢氧根离子含有10个电子,0.1molOH-含有0.1mol×10×NA=NA个电子,故C正确;
D.5.6g金属铁物质的量为0.1mol,和足量盐酸反应,失去的电子数目为0.2NA,故D错误;
故选:BC.
点评:本题考查阿伏加德罗常数的有关计算和判断,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系是解题关键,注意气体摩尔体积的使用条件.

练习册系列答案
相关题目
NA为阿伏加德罗常数,下列说法正确的是( )
| A、标准状况下,11.2L的戊烷所含的分子数为0.5NA |
| B、26g乙炔所含共用电子对数目为2NA |
| C、标准状况下,11.2L CCl4所含分子数为0.5NA |
| D、现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3NA |
量取20mL的水,应该选用的仪器是( )
| A、10 mL量筒 |
| B、50 mL量筒和胶头滴管 |
| C、25 mL量筒和胶头滴管 |
| D、托盘天平称量 |
下列各溶液中,Na+ 浓度最大的是( )
| A、1 L 1.2 mol?L-1的NaCl溶液 |
| B、2 L 1 mol?L-1的NaOH溶液 |
| C、0.5 L 0.8 mol?L-1的Na2SO4溶液 |
| D、3 L 0.5 mol?L-1的Na2CO3溶液 |
 50mL 0.50mol?L-1盐酸与50mL 0.55mol?L-1 NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中的热量可计算中和热.回答下列问题:
50mL 0.50mol?L-1盐酸与50mL 0.55mol?L-1 NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中的热量可计算中和热.回答下列问题: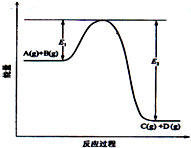 反应A(g)+B(g) 错误!未找到引用源C(g)+D(g)过程中的能量变化如图所示,请回答下列问题:
反应A(g)+B(g) 错误!未找到引用源C(g)+D(g)过程中的能量变化如图所示,请回答下列问题:
 将一定量的Mg、Al投入100mL一定的物质的量浓度的盐酸中,合金全部溶解.向所得溶液中滴加5mol/L的NaOH至过量,生成的沉淀的质量与加入NaOH的体积的关系如图所示.
将一定量的Mg、Al投入100mL一定的物质的量浓度的盐酸中,合金全部溶解.向所得溶液中滴加5mol/L的NaOH至过量,生成的沉淀的质量与加入NaOH的体积的关系如图所示.