题目内容
印刷电路板是由塑料和铜箔复合而成,刻制印刷电路时要用FeCl3溶液作为“腐蚀液”生成CuCl2和FeCl2,其反应的化学方程式如下:Cu+2FeCl3═CuCl2+2FeCl2
(1)请在上式中标出电子转移的方向和数目
(2)该反应的氧化剂是 ,氧化产物是 .
(3)写出FeCl3的电离方程式: .
(1)请在上式中标出电子转移的方向和数目
(2)该反应的氧化剂是
(3)写出FeCl3的电离方程式:
考点:氧化还原反应
专题:氧化还原反应专题
分析:(1)根据氧化还原反应中化合价的升降来分析电子转移情况;
(2)化合价降低元素所在的反应物是氧化剂,还原剂被氧化得到的产物为氧化产物;
(3)FeCl3为强电解质在溶液中完全电离.
(2)化合价降低元素所在的反应物是氧化剂,还原剂被氧化得到的产物为氧化产物;
(3)FeCl3为强电解质在溶液中完全电离.
解答:
解:(1)反应Cu+2FeCl3═CuCl2+2FeCl2中,化合价升高元素是铜,化合价降低的元素是铁,共转移电子2mol,转移电子方向和数目为 ,故答案为:
,故答案为: ;
;
(2)Cu+2FeCl3═CuCl2+2FeCl2反应中化合价降低元素是铁,所在的反应物是FeCl3,为氧化剂,Cu的化合价升高被氧化,生成产物CuCl2为氧化产物,
故答案为:FeCl3;CuCl2;
(3)FeCl3为强电解质在溶液中完全电离,其电离方程式为:FeCl3=Fe3++3Cl-,故答案为:FeCl3=Fe3++3Cl-.
 ,故答案为:
,故答案为: ;
;(2)Cu+2FeCl3═CuCl2+2FeCl2反应中化合价降低元素是铁,所在的反应物是FeCl3,为氧化剂,Cu的化合价升高被氧化,生成产物CuCl2为氧化产物,
故答案为:FeCl3;CuCl2;
(3)FeCl3为强电解质在溶液中完全电离,其电离方程式为:FeCl3=Fe3++3Cl-,故答案为:FeCl3=Fe3++3Cl-.
点评:本题以铁离子为依托重点考查氧化还原反应原理和电解质的电离,侧重于氧化还原反应理论的应用,题目难度不大,注意从元素化合价的角度认识相关概念和物质的性质.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列叙述正确的是( )
| A、工业上用电解熔融氯化铝和冰晶石的混合物的方法得到铝 |
| B、一次电池是最常见的化学电源,一次电池中发生氧化还原反应的物质大部分被消耗后就不能再使用,铅蓄电池是最常见的一次电池 |
| C、氯碱工业中,氢氧化钠在电解槽的阴极区产生 |
| D、合成氨生产中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
化学与生产、生活、环境等社会实际密切相关.下列叙述正确的是( )
| A、航天飞机上的隔热陶瓷瓦属于复合材料 |
| B、推广使用煤液化技术,可减少二氧化碳等温室气体的排放 |
| C、氧化铝是冶炼金属铝的原料,也是一种比较好的耐火材料 |
| D、半导体行业中有一句话:“从沙滩到用户”,计算机芯片的材料是二氧化硅 |
关于氧化剂的叙述正确的是( )
| A、分子中不一定含有氧元素 |
| B、分子中一定含有氧元素 |
| C、在反应中有元素化合价升高 |
| D、在反应中有元素化合价降低 |
下列离子方程式或化学反应方程式与所述事实相符且正确的是( )
| A、将少量SO2气体通入NaClO溶液中:SO2+H2O+2ClO-=SO32-+2HClO |
| B、将2molSO3气体通入一密闭容器中,达平衡后吸收QkJ热量,则该反应的热化学方程式为:2SO3(g)?2SO2(g)+O2(g)△H=+Q kJ/mol |
| C、向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反应:4Fe2++2Br-+3Cl2=4Fe3++6Cl-+Br2 |
| D、NH4Al(SO4)2溶液中加入Ba(OH)2溶液使SO42-完全沉淀:Al3++2SO42-+2Ba2++4OH-=AlO2-+2BaSO4↓+2H2O |
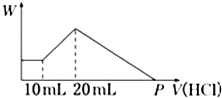 把由NaOH、AlCl3、MgCl2三种固体组成的混合物,溶于足量水中后有0.58 g白色沉淀生成,在所得的浑浊液中,逐滴加入0.5 mol/L盐酸,加入盐酸的体积(V)与生成沉淀的质量(W)关系如图所示:
把由NaOH、AlCl3、MgCl2三种固体组成的混合物,溶于足量水中后有0.58 g白色沉淀生成,在所得的浑浊液中,逐滴加入0.5 mol/L盐酸,加入盐酸的体积(V)与生成沉淀的质量(W)关系如图所示: