题目内容
元素化合物的知识是中学化学的重要知识,请结合有关知识回答下列问题:
(1)NaHCO3是发酵粉的主要成分之一,主要是利用其受热易分解的性质,请写出该反应的化学方程式:
(2)实验室的浓硝酸需用棕色瓶储存并置于冷暗处其原因是(用化学方程式说明)
(3)治疗胃酸过多常服用氢氧化铝,其药理是: (用离子方程式说明)
(4)写出铝粉和氧化铁发生铝热反应的化学方程式 ,铝热反应常用于生产上,请你举出一例用途 .
(1)NaHCO3是发酵粉的主要成分之一,主要是利用其受热易分解的性质,请写出该反应的化学方程式:
(2)实验室的浓硝酸需用棕色瓶储存并置于冷暗处其原因是(用化学方程式说明)
(3)治疗胃酸过多常服用氢氧化铝,其药理是:
(4)写出铝粉和氧化铁发生铝热反应的化学方程式
考点:钠的重要化合物,硝酸的化学性质,铝的化学性质,两性氧化物和两性氢氧化物
专题:
分析:(1)碳酸氢钠不稳定受热分解生成碳酸钠和二氧化碳和水;
(2)浓硝酸不稳定,见光易分解;
(3)氢氧化铝与盐酸发生酸碱中和反应,消耗氢离子;
(4)铝与氧化铁饭生成铁与氧化铝.
(2)浓硝酸不稳定,见光易分解;
(3)氢氧化铝与盐酸发生酸碱中和反应,消耗氢离子;
(4)铝与氧化铁饭生成铁与氧化铝.
解答:
解:(1)碳酸氢钠不稳定受热分解生成碳酸钠和二氧化碳和水,化学方程式为:2NaHCO3
Na2CO3+CO2↑+H2O;
故答案为:2NaHCO3
Na2CO3+CO2↑+H2O;
(2)浓硝酸不稳定,见光易分解,化学方程式为:4HNO3
4NO2↑+O2↑+2H2O;
故答案为:4HNO3
4NO2↑+O2↑+2H2O;
(3)治疗胃酸过多常服用氢氧化铝,发生反应的化学方程式为:Al(OH)3+3H+=Al3++3H2O;
故答案为:Al(OH)3+3H+=Al3++3H2O;
(4)铝粉和氧化铁发生铝热反应的化学方程式:2Al+Fe2O3
2Fe+Al2O3;铝热反应能够用于焊接钢轨;
故答案为:2Al+Fe2O3
2Fe+Al2O3;焊接钢轨;
| ||
故答案为:2NaHCO3
| ||
(2)浓硝酸不稳定,见光易分解,化学方程式为:4HNO3
| ||
故答案为:4HNO3
| ||
(3)治疗胃酸过多常服用氢氧化铝,发生反应的化学方程式为:Al(OH)3+3H+=Al3++3H2O;
故答案为:Al(OH)3+3H+=Al3++3H2O;
(4)铝粉和氧化铁发生铝热反应的化学方程式:2Al+Fe2O3
| ||
故答案为:2Al+Fe2O3
| ||
点评:本题考查了化学方程式、离子方程式的书写,明确物质的性质和发生的反应是解题关键,注意药品保存的方法.

练习册系列答案
相关题目
一定温度下,反应N2(g)+3H2(g)?2NH3(g)达到化学平衡状态的标志是( )
| A、N2、H2和NH3的物质的量分数不再改变 |
| B、c(N2):c(H2):c(NH3)=1:3:2 |
| C、单位时间每增加1molN2,同时增加2mol NH3 |
| D、N2与H2的物质的量之和是NH3的2倍 |
电子表所用的纽扣电池的两极材料为锌和氧化银,电解质溶液为KOH溶液,其电极反应式是:Zn+2OH--2e-═ZnO+H2O; Ag2O+H2O+2e-═2Ag+2OH- 下列说法正确的是( )
| A、Zn为正极,Ag2O为负极 |
| B、Ag2O发生还原反应 |
| C、原电池工作时,正极区溶液pH值减小 |
| D、原电池工作时,负极区溶液pH值增大 |
某原电池装置如图所示,盐桥中装有用饱和氯化钾溶液浸泡过的琼脂.下列叙述正确的是( )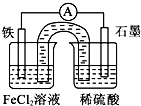

| A、原电池工作一段时间后,FeCl2溶液中c(Cl-)会增大 |
| B、Fe为负极,发生的反应为:Fe-3e-=Fe3+ |
| C、Fe为正极,石墨上发生的反应为:2H++2e-═H2↑ |
| D、原电池装置中的盐桥完全可用金属导线代替 |
下列氯化物中,能直接利用对应的金属单质与稀盐酸反应得到的是( )
| A、FeCl3 |
| B、CuCl2 |
| C、AgCl |
| D、AlCl3 |
下列离子方程式书写正确的是( )
| A、向碳酸钠溶液中滴加与其溶质的物质的量相等的盐酸:CO32-+2H+═CO2↑+H2O |
| B、用Na2S处理含Hg 2+的废水:Hg2++S2-═HgS↓ |
| C、用Na2CO3溶液处理水垢中的CaSO4:Ca2++CO32-═CaCO3 |
D、邻羟基苯甲酸与足量的NaOH溶液混合: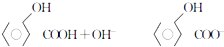 +H2O +H2O |