题目内容
按如图所示装置进行下列不同的操作,说法不正确的是( )


| A、只接通K3,一段时间后,漏斗液面上升 |
| B、只接通K1,一段时间后,U形管中出现白色沉淀 |
| C、只接通K2,U形管左、右两端液面均下降 |
| D、铁腐蚀的速度由大到小的顺序是:只接通K1>只接通K3>都断开>只接通K2 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:A.只接通K3,该装置为原电池,铁发生吸氧腐蚀;
B.只接通K1,该装置为电解池,铁作阳极,石墨作阴极,阳极上铁失电子发生氧化反应,阴极上氢离子放电;
C.只接通K2,该装置为电解池,铁作阴极,石墨作阳极,阳极上氯离子放电,阴极上氢离子放电;
D.铁腐蚀快慢规律是:作电解池阳极>作原电池负极>化学腐蚀>作原电池正极>作电解池阴极.
B.只接通K1,该装置为电解池,铁作阳极,石墨作阴极,阳极上铁失电子发生氧化反应,阴极上氢离子放电;
C.只接通K2,该装置为电解池,铁作阴极,石墨作阳极,阳极上氯离子放电,阴极上氢离子放电;
D.铁腐蚀快慢规律是:作电解池阳极>作原电池负极>化学腐蚀>作原电池正极>作电解池阴极.
解答:
解:只接通K3,该装置为原电池,铁发生吸氧腐蚀,石墨电极上氧气得电子生成氢氧根离子,则压强减小,所以一段时间后,漏斗液面下降,故A错误;
B.只接通K1,该装置为电解池,铁作阳极,石墨作阴极,阳极上铁生成亚铁离子,阴极上氢离子放电同时生成氢氧根离子,亚铁离子和氢氧根离子反应生成氢氧化亚铁白色沉淀,故B正确;
C.只接通K2,该装置为电解池,铁作阴极,石墨作阳极,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,所以U形管左、右两端液面均下降,故C正确;
D.铁腐蚀快慢规律是:作电解池阳极>作原电池负极>化学腐蚀>作原电池正极>作电解池阴极,所以铁腐蚀的速度由大到小的顺序是:只接通K1>只接通K3>都断开>只接通K2,故D正确;
故选A.
B.只接通K1,该装置为电解池,铁作阳极,石墨作阴极,阳极上铁生成亚铁离子,阴极上氢离子放电同时生成氢氧根离子,亚铁离子和氢氧根离子反应生成氢氧化亚铁白色沉淀,故B正确;
C.只接通K2,该装置为电解池,铁作阴极,石墨作阳极,阳极上氯离子放电生成氯气,阴极上氢离子放电生成氢气,所以U形管左、右两端液面均下降,故C正确;
D.铁腐蚀快慢规律是:作电解池阳极>作原电池负极>化学腐蚀>作原电池正极>作电解池阴极,所以铁腐蚀的速度由大到小的顺序是:只接通K1>只接通K3>都断开>只接通K2,故D正确;
故选A.
点评:本题考查了原电池和电解池原理,明确各个电极上发生的反应是解本题关键,再结合物质间的反应分析解答,注意:活泼金属作阳极时,阳极上金属失电子而不是阴离子失电子,为易错点.

练习册系列答案
相关题目
 将如图所示实验装置的K闭合,下列判断正确的是( )
将如图所示实验装置的K闭合,下列判断正确的是( )| A、电子沿Zn→a→b→Cu路径流动 |
| B、Cu电极上发生还原反应 |
| C、片刻后甲池中c(SO42-)增大 |
| D、片刻后可观察到滤纸b点变红色 |
下列操作错误的是( )(填序号)
| A、用蒸发皿进行加热蒸发实验时,不垫石棉网 |
| B、浓硫酸不慎沾到皮肤上,迅速用NaOH溶液清洗,再用水洗 |
| C、蒸馏时,将温度计水银球插入液面以下 |
| D、闻气体气味时,用手在容器口轻轻扇动,使少量气体飘入鼻孔中 |
| E、使用分液漏斗和容量瓶时,首先检查是否漏水 |
酒后驾车人员体内酒精含量的检测装置如图所示,下列说法正确的是( )


| A、该检测装置实现了将化学能转化为电能,且单位时间内通过电量越大,酒精含量越高 |
| B、电极A是正极 |
| C、电极B的反应:H2O+C2H5OH-4e-=CH3COOH+4H+ |
| D、电池总反应:O2+C2H5OH=CH3COOH+H2O |
对实验Ⅰ~Ⅳ的实验现象判断正确的是( )
A、 实验Ⅰ:产生红褐色沉淀 |
B、 实验Ⅱ:试管中溶液变红色 |
C、 实验Ⅲ:试管中溶液变红色 实验Ⅲ:试管中溶液变红色 |
D、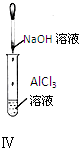 实验Ⅳ:试管中先出现白色沉淀,后溶解 |
下列化学式一定表示一种物质的是( )
| A、CF2Cl2 |
| B、C6H12O6 |
| C、C12H22O11 |
| D、C2H4O2 |
 铜、铁、钒都是日常生活中常见的金属,具有广泛用途.
铜、铁、钒都是日常生活中常见的金属,具有广泛用途.