题目内容
如图为某市售盐酸试剂瓶上的部分数据.
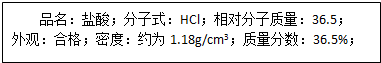
(1)该市售盐酸的物质的量浓度为 .
(2)在标准状况下,1体积水吸收 体积的HCl气体可制得上述盐酸.(水的密度以1.00g/cm3计)

(1)该市售盐酸的物质的量浓度为
(2)在标准状况下,1体积水吸收
考点:物质的量浓度的相关计算
专题:计算题
分析:(1)根据c=
计算该盐酸的物质的量浓度;
(2)令水的体积为1L,HCl的体积为xL,根据n=
计算HCl的物质的量,根据m=nM计算HCl的质量,根据m=ρV计算水的质量,根据m(溶质)=m(溶液)×w(溶质)列方程解答.
| 1000ρw |
| M |
(2)令水的体积为1L,HCl的体积为xL,根据n=
| V |
| Vm |
解答:
解:(1)密度为1.18g/mL、质量分数为36.5%的浓盐酸的物质的量为:
mol/L=11.8mol/L,
故答案为:11.8 mol/L;
(2)令水的体积为1L,HCl的体积为xL,则:
HCl的物质的量=
=
mol,HCl的质量=
mol×36.5g/mol=
g,1L水的质量=1000mL×1g/mL=1000g,
故(1000g+
g)×36.5%=
g,解得x=352.8,
故答案为:352.8.
| 1000×1.18×36.5% |
| 36.5 |
故答案为:11.8 mol/L;
(2)令水的体积为1L,HCl的体积为xL,则:
HCl的物质的量=
| x L |
| 22.4L/mol |
| x |
| 22.4 |
| x |
| 22.4 |
| 36.5x |
| 22.4 |
故(1000g+
| 36.5x |
| 22.4 |
| 36.5x |
| 22.4 |
故答案为:352.8.
点评:本题考查溶液浓度有关计算,涉及物质的量浓度、质量分数,注意对公式的理解与灵活应用.

练习册系列答案
相关题目
下列有关物质的用途叙述正确的是( )
| A、陶瓷史人类应用很早的硅酸盐材料 |
| B、实验室中浓硝酸应保存在带有橡胶塞的无色玻璃瓶中 |
| C、高温下铁可以和水蒸气反应,生成红褐色的Fe(OH)3 |
| D、Na2O2具有强氧化性,具有杀菌能力,可用于饮用水的消毒 |
下列说法正确的是( )
| A、室温下,在水中的溶解度:丙三醇>苯酚>1-氯丁烷 |
| B、用核磁共振氢谱不能区分HCOOCH3和HCOOCH2CH3 |
| C、用Na2CO3溶液不能区分CH3COOH和CH3COOCH2CH3 |
| D、油脂在酸性或碱性条件下均可发生水解反应,且产物相同 |
 A、B、C、D是由下面的一种阳离子和一种阴离子组成的化合物(阳离子:NH4+、Na+、H+,阴离子:Cl-、CH3COO -、OH-),在水溶液中A、D能促进水的电离,B、C能抑制水的电离.常温下各物质从1mL稀释到100mL,pH的变化如图Ⅰ所示,请回答:
A、B、C、D是由下面的一种阳离子和一种阴离子组成的化合物(阳离子:NH4+、Na+、H+,阴离子:Cl-、CH3COO -、OH-),在水溶液中A、D能促进水的电离,B、C能抑制水的电离.常温下各物质从1mL稀释到100mL,pH的变化如图Ⅰ所示,请回答: