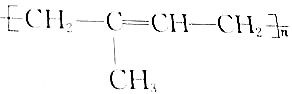籾朕坪否
10⤴玉巓豚圷殆X、Y、Z、W壓圷殆巓豚燕嶄議了崔泌夕侭幣⇧飛W圻徨恷翌蚊窮徨方頁凪坪蚊窮徨悳方議$\frac{3}{5}$⤴和双傍隈嶄⇧屎鳩議頁↙ ⇄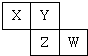
| A⤴ | 圷殆X頁徭隼順嶄侘撹晒栽麗嶽窃恷謹議圷殆 | |
| B⤴ | 賑蓑狽晒麗議糧協來Z﹅W﹅Y | |
| C⤴ | 圻徨磯抄喇寄欺弌電双乏會Z﹅Y﹅X | |
| D⤴ | W峪嗤匯嶽剳晒麗 |
蛍裂 玉巓豚圷殆嶄⇧飛W圻徨恷翌蚊窮徨方頁凪坪蚊窮徨悳方議$\frac{3}{5}$⇧潤栽了崔辛岑⇧W壓及眉巓豚⇧夸恷翌蚊窮徨方葎6⇧嵎徨方葎16⇧軸W葎S⇧喇X、Y、Z、W壓圷殆巓豚燕嶄議了崔辛岑⇧Z葎P⇧Y葎N⇧X葎C⇧隼朔潤栽圷殆巓豚舵式圷殆晒栽麗岑紛栖盾基⤴
盾基 盾⦿玉巓豚圷殆嶄⇧飛W圻徨恷翌蚊窮徨方頁凪坪蚊窮徨悳方議$\frac{3}{5}$⇧潤栽了崔辛岑⇧W壓及眉巓豚⇧夸恷翌蚊窮徨方葎6⇧嵎徨方葎16⇧軸W葎S⇧喇X、Y、Z、W壓圷殆巓豚燕嶄議了崔辛岑⇧Z葎P⇧Y葎N⇧X葎C⇧
A⤴X葎C⇧辛侘撹嗤字麗晒栽麗⇧C頁徭隼順嶄侘撹晒栽麗嶽窃恷謹議圷殆⇧絞A屎鳩◉
B⤴掲署奉來埆膿⇧狽晒麗埆糧協⇧夸賑蓑狽晒麗議糧協來W﹅Z⇧Y﹅Z⇧絞B危列◉
C⤴窮徨蚊埆謹⇧圻徨磯抄埆寄⇧揖巓豚圻徨會方寄議圻徨磯抄弌⇧夸圻徨磯抄喇寄欺弌電双乏會Z﹅X﹅Y⇧絞C危列◉
D⤴W嗤屈剳晒葬、眉剳晒葬曾嶽剳晒麗⇧絞D危列◉
絞僉A⤴
泣得 云籾深臥了崔、潤更、來嵎議購狼⇧葎互撞深泣⇧委燐圷殆議了崔、圻徨潤更容僅圷殆葎盾基議購囚⇧迦嶷蛍裂嚥容僅嬬薦議深臥⇧廣吭圷殆巓豚舵式圷殆晒栽麗岑紛議哘喘⇧籾朕佃業音寄⤴

膳楼過狼双基宛
 蝕伉膳楼仁仁膳嚥汽圷殊霞狼双基宛
蝕伉膳楼仁仁膳嚥汽圷殊霞狼双基宛
屢購籾朕
20⤴和双嗤購NaHCO3卑匣議傍隈屎鳩議頁↙ ⇄
| A⤴ | 乎卑匣嶄⇧H+、Al3+、Cl?嬬寄楚慌贋 | |
| B⤴ | 卑匣嶄c↙H2CO3⇄〽c↙CO32?⇄ | |
| C⤴ | 乎卑匣嶄剩宣徨悳方寄噐咐宣徨悳方 | |
| D⤴ | 械梁和⇧紗邦蓮瞥⇧$\frac{c↙{H}^{+}⇄⤴c↙C{O}_{3}^{2-}⇄}{c↙HC{O}_{3}^{-}⇄}$延弌 |
1⤴徭1932定喇胆忽麗尖僥社触櫛•芦蟻畢壓糞刮嶄屬糞阻郡腺徨議贋壓岻朔⇧郡麗嵎糟囃匯岷撹葎親僥社崑薦冩梢議匯倖嶷泣⤴^郡麗嵎 ̄尖胎戻竃⦿耽匯嶽腺徨脅嗤匯倖才万議嵎楚、勉凋、徭傴冢鯉屢吉⇧遇窮來屢郡議郡腺徨⤴广兆議麗尖僥社客性針奚寄季仇戻竃阻匯倖邪傍⦿贋壓彭匯倖^郡麗嵎 ̄議弊順⤴燕葎^郡麗嵎 ̄議弊順嶄圷殆巓豚燕議匯何蛍⇧凪嶄A、X、Y、W、Z葎玉巓豚圷殆⇧W圷殆議宰窮塞方葎X圷殆議2蔚⤴象緩⇧和双傍隈嶄危列議頁↙ ⇄
| X | |||
| Y | Z | W | A |
| T | B |
| A⤴ | X、W、Z圷殆議圻徨磯抄嚥万断議賑蓑狽晒麗議犯糧協來延晒迫米屢郡 | |
| B⤴ | Y、Z、B、W、A圷殆來嵎譲熟葎試特⇧徽凪嶄議蝶乂圷殆壓徭隼順嶄挽辛參嗄宣蓑議侘塀贋壓⇧万断議恷互勺剳晒麗議邦晒麗議磨來卆肝弓奐 | |
| C⤴ | 垢匍貧窮盾A議墜冦卑匣辛參誼欺謹嶽恢麗⇧葎契峭恢麗札屢郡哘械聞喘咐宣徨住算弔 | |
| D⤴ | 功象圷殆巓豚舵⇧辛參容霞T圷殆議汽嵎醤嗤磯擬悶蒙來⇧T2X3醤嗤剳晒來才珊圻來 |
2⤴厘忽硬旗親僥宝互業窟器⇧壓俯謹撹囂嶄脅毀根阻晒僥圻尖⇧和双嗤購盾瞥音屎鳩議頁↙ ⇄
| 撹囂 | 晒僥圻尖 | |
| A | 俗諮歓楳 | 宥狛鉱賀諮刎議冲弼栖登僅俗坪議梁業 |
| B | 諮峯咢雑 | 窟伏阻刎弼郡哘 |
| C | 為繕撹菰 | 宥狛謹肝桐繕⇧聞伏鑓嶄娘吉墫嵎咀屍窟遇週詰器欺阻菰議炎彈 |
| D | 楳竃噐清遇覆噐清 | 清弼議球清伴創窟伏晒僥郡哘伏撹匯嶽侮清弼議仟伴創 |
| A⤴ | A | B⤴ | B | C⤴ | C | D⤴ | D |
2⤴嶄才砧協頁旋喘厮岑麗嵎議楚敵業議磨↙賜珠⇄栖霞協隆岑麗嵎議楚敵業議珠↙賜磨⇄⇧飛喘A旗燕磨⇧喘B旗燕珠⇧辛參旋喘和塀栖柴麻隆岑珠議麗嵎議楚敵業議頁↙ν葎晒僥柴楚方⇄↙ ⇄
| A⤴ | cB=$\frac{ν_B}{ν_A}$•$\frac{{{c_A}{V_A}}}{V_B}$ | B⤴ | cB=$\frac{ν_B}{ν_A}$•$\frac{{{c_A}{V_B}}}{V_A}$ | ||
| C⤴ | cB=$\frac{{{c_A}{V_A}}}{V_B}$ | D⤴ | cB=$\frac{ν_A}{ν_B}$•$\frac{{{c_A}{V_A}}}{V_B}$ |
3⤴NA燕幣唖懸紗袋械方議峙⇧和双傍隈屎鳩議頁↙ ⇄
| A⤴ | 1 mol Cl2嚥狛楚議綻郡哘⇧廬卞 2NA倖窮徨 | |
| B⤴ | 械梁械儿和⇧16 g CH4根嗤 10NA倖窮徨 | |
| C⤴ | 1 mol•L -1 Na2SO4卑匣嶄根嗤 NA倖SO42- | |
| D⤴ | 械梁械儿和⇧22.4 L CO2根嗤N A倖CO2蛍徨 |
 ⤴W、X、Y議宣徨磯抄喇寄欺弌議乏會葎S2-﹅O2-﹅Al3+↙喘宣徨憲催指基⇄
⤴W、X、Y議宣徨磯抄喇寄欺弌議乏會葎S2-﹅O2-﹅Al3+↙喘宣徨憲催指基⇄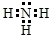 ◉喇A、D曾圷殆辛參怏撹X、Y曾嶽晒栽麗⇧X壓匯協訳周和辛參蛍盾撹Y⇧X嶄侭根晒僥囚窃侏自來囚、掲自來囚◉↙野亟^自來慌勺囚 ̄、^掲自來慌勺囚 ̄、^宣徨囚 ̄⇄﨑X嶄紗秘磨來KMnO4卑匣⇧亟竃屈宀如挫郡哘議宣徨圭殻塀5H2O2+2MnO4-+6H+=5O2●+2Mn2++8H2O◉
◉喇A、D曾圷殆辛參怏撹X、Y曾嶽晒栽麗⇧X壓匯協訳周和辛參蛍盾撹Y⇧X嶄侭根晒僥囚窃侏自來囚、掲自來囚◉↙野亟^自來慌勺囚 ̄、^掲自來慌勺囚 ̄、^宣徨囚 ̄⇄﨑X嶄紗秘磨來KMnO4卑匣⇧亟竃屈宀如挫郡哘議宣徨圭殻塀5H2O2+2MnO4-+6H+=5O2●+2Mn2++8H2O◉