题目内容
下列实验能成功的是( )
| A、将乙酸和乙醇混合加热制乙酸乙酯 |
| B、苯和浓溴水反应制溴苯 |
| C、CH3CH2Br中滴加AgNO3溶液观察是否有浅黄色沉淀,判断卤代烃的类型 |
| D、用CuSO4溶液和过量NaOH溶液混合,然后加入几滴乙醛,加热煮沸观察红色沉淀 |
考点:化学实验方案的评价
专题:
分析:A.制备乙酸乙酯需要浓硫酸;
B.苯和浓溴水不反应;
C.CH3CH2Br中不能电离出溴离子;
D.反应生成氢氧化铜,在NaOH碱性条件下可与乙醛发生氧化反应.
B.苯和浓溴水不反应;
C.CH3CH2Br中不能电离出溴离子;
D.反应生成氢氧化铜,在NaOH碱性条件下可与乙醛发生氧化反应.
解答:
解:A.制备乙酸乙酯需要浓硫酸,缺少浓硫酸作催化剂、吸水剂,不能制备,故A错误;
B.苯和浓溴水不反应,应选苯与液溴、铁粉制备溴苯,故B错误;
C.CH3CH2Br中不能电离出溴离子,与AgNO3溶液不反应,故C错误;
D.反应生成氢氧化铜,在NaOH碱性条件下可与乙醛发生氧化反应,加热煮沸可观察到红色沉淀,故D正确;
故选D.
B.苯和浓溴水不反应,应选苯与液溴、铁粉制备溴苯,故B错误;
C.CH3CH2Br中不能电离出溴离子,与AgNO3溶液不反应,故C错误;
D.反应生成氢氧化铜,在NaOH碱性条件下可与乙醛发生氧化反应,加热煮沸可观察到红色沉淀,故D正确;
故选D.
点评:本题考查化学实验方案的评价,为高频考点,把握物质的性质、有机物制备实验等为解答的关键,侧重物质性质及实验基本技能的考查,题目难度不大.

练习册系列答案
相关题目
镍镉(Ni-Cd)可充电电池在现代生活中有广泛应用,它的充放电反应按下式进行:Cd(OH)2+2Ni(OH)2
Cd+2NiO(OH)+2H2O由此可知,该电池放电时的负极材料是( )
| 充电 |
| 放电 |
| A、Cd(OH)2 |
| B、Ni(OH)2 |
| C、Cd |
| D、NiO(OH) |
下列物质性质与相应结果或应用的对应关系正确的是( )
| A、酸性越强的含氧酸跟铁片反应产生氢气越快 |
| B、将草木灰和硫铵混合施用,可使肥效更高 |
| C、Mg(OH)2和Al(OH)3受热易分解,常用它们作阻燃剂 |
| D、某地雨水经过一段时间,其pH由4.68降为4.28,因为水中溶解了较多的CO2 |
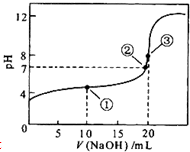 常温下,用0.1mol?L-1 NaOH溶液滴定20mL 0.1mol?L-1CH3COOH溶液的滴定曲线如图所示.下列说法正确的是( )
常温下,用0.1mol?L-1 NaOH溶液滴定20mL 0.1mol?L-1CH3COOH溶液的滴定曲线如图所示.下列说法正确的是( )| A、点①所示溶液中:c(Na+)>c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-) | ||
| B、点②所示溶液中:c(Na+)+c(H+)=c(CH3COO-)+c(CH3COOH)+c(OH-) | ||
| C、点③所示溶液中:c(CH3COO-)>c(Na+)>c(OH-)>c(H+) | ||
D、在整个滴定过程中:溶液中
|
化学实验中常将溶液或试剂进行酸化,下列酸化处理的措施正确的是( )
| A、检验溶液是否含有SO42-时,先用盐酸将待检验溶液酸化,然后往其中滴加BaCl2溶液 |
| B、为提高高锰酸钾溶液的氧化能力,用盐酸将高锰酸钾溶液酸化 |
| C、检验溶液中是否含有Fe3+时,用硝酸酸化 |
| D、定性检验SO32-,将BaCl2溶液用HNO3酸化 |
配制0.50mol?L-1的NaOH溶液245ml,下列操作正确的是( )
| A、用托盘天平称取4.9gNaOH固体 |
| B、NaOH固体加蒸馏水溶解,要待溶液冷却到室温后,再转移至容量瓶中 |
| C、容量瓶不能用玻璃瓶塞、应用塑料瓶塞 |
| D、定容摇匀后发现溶液体积低于刻度线,再补加少量蒸馏水至刻度线 |
某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5,其主要来源是化石燃料的燃烧.下列物质中,不属于化石燃料的是( )
| A、煤 | B、石油 | C、天然气 | D、氢气 |

