题目内容
某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5,其主要来源是化石燃料的燃烧.下列物质中,不属于化石燃料的是( )
| A、煤 | B、石油 | C、天然气 | D、氢气 |
考点:使用化石燃料的利弊及新能源的开发
专题:
分析:化石燃料是指远古的动植物在地底下经过几亿年的时间形成的燃料,据此分析.
解答:
解:化石燃料是指远古的动植物在地底下经过几亿年的时间形成的燃料,包括煤、石油和天然气,故选D.
点评:本题考查了化石燃料的分类,属于识记型题目,难度不大.

练习册系列答案
相关题目
下列实验能成功的是( )
| A、将乙酸和乙醇混合加热制乙酸乙酯 |
| B、苯和浓溴水反应制溴苯 |
| C、CH3CH2Br中滴加AgNO3溶液观察是否有浅黄色沉淀,判断卤代烃的类型 |
| D、用CuSO4溶液和过量NaOH溶液混合,然后加入几滴乙醛,加热煮沸观察红色沉淀 |
已知在热的碱性溶液中,NaClO发生如下反应:3NaClO=2NaCl+NaClO3,在相同条件下NaClO2也能发生类似的反应,其最终产物是( )
| A、NaCl、NaClO |
| B、NaCl、NaClO3 |
| C、NaClO、NaClO3 |
| D、NaClO3、NaClO4 |
常温下,在溶液中可发生以下反应:①2Fe2++Br2═2Fe3++2Br-②2Br-+Cl2═Br2+2Cl-③2Fe3++2I-═2Fe2++2I2由此判断下列说法正确的是( )
| A、铁元素在反应①和③中均被氧化 |
| B、Fe2+在氧化还原反应中只能做还原剂 |
| C、还原性强弱顺序为:I->Br->Fe2+>Cl- |
| D、反应③中当有2molFe3+ 被还原时,有2mol I-被氧化 |
常温时,下列各组离子在指定溶液中,能大量共存的是( )
| A、pH=11的溶液中:Na+、[Al(OH)4]-、S2-、SO32- |
| B、水电离的浓度为 10-12mol?L-1的溶液中:Cl-、CO32-、NH4+、SO32- |
| C、使石蕊变红的溶液中:Fe2+、MnO4-、Na+、SO42- |
| D、中性溶液中:Fe3+、Al3+、I-、S2- |
据报道,最近摩托罗拉公司研发了一种由甲醇和氧气以及强碱做电解质溶液的新型手机电池,电量可达现在使用的镍氢电池或锂电池的十倍,可连续使用一个月才充一次电.其电池反应为:2CH3OH+3O2+4OH-═2CO32-+6H2O,则下列说法错误的是( )
| A、放电时CH3OH参与反应的电极为正极 |
| B、充电时电解质溶液的pH逐渐增大 |
| C、放电时负极的电极反应为:CH3OH-6e-+8OH-=CO32-+6H2O |
| D、充电时每生成1 mol CH3OH转移6 mol电子 |
常见镍氢电池的某极是储氢合金LaNi5H6 (LaNi5H6中各元素化合价均为零),电池反应通常表示为LaNi5H6+6NiO(OH)2
LaNi5+6Ni(OH)3下列说法不正确的是( )
| 放电 |
| 充电 |
| A、放电时储氢合金作负极 |
| B、充电是将电能转化为化学能的过程 |
| C、充电时储氢合金作阴极 |
| D、1mol LaNi5H6参加放电,能提供12mol电子 |
下列有关化学用语的表示正确的是( )
A、质量数为37的氯原子:
| ||
B、二氧化碳分子的比例模型: | ||
C、NH4Br的电子式: | ||
D、对羟基苯甲醛的结构简式: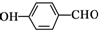 |