题目内容
13.在下列可逆反应中,增大压强或降低温度,均可使化学平衡向正反应方向移动的是( )| A. | 2SO2(g)+O2(g)?2SO3(g)(正反应是放热反应) | |
| B. | 4NH3(g)+5O2(g)?4NO(g)+6H2O(g)(正反应是放热反应) | |
| C. | 2NH3(g)?N2(g)+3H2(g)(正反应是吸热反应) | |
| D. | SO2(g)+NO2(g)?SO3(g)+NO(g)(正反应是放热反应) |
分析 增大压强或降低温度,均可使化学平衡向正反应方向移动,可知反应为气体体积减小、放热的反应,以此来解答.
解答 解:A.为气体体积减小、放热的反应,则增大压强或降低温度,均可使化学平衡向正反应方向移动,故A选;
B.为气体体积增大的反应,增大压强平衡逆向移动,故B不选;
C.为气体体积增大的反应,增大压强平衡逆向移动,且为吸热反应,升高温度平衡逆向移动,故C不选;
D.为气体体积不变的反应,增大压强平衡不移动,故D不选;
故选A.
点评 本题考查化学平衡的移动,为高频考点,把握压强、温度对平衡移动的影响为解答的关键,侧重分析与应用能力的考查,注意反应的特点,题目难度不大.

练习册系列答案
相关题目
1.下列离子方程式中,正确的是( )
| A. | KI的酸性溶液长期置于空气中:4I-+2H2O+O2═2I2+4OH- | |
| B. | 高锰酸钾酸性溶液与草酸溶液反应:2MnO4-+5C2O42-+16H+═2Mn2++10CO2↑+8H2O | |
| C. | 用稀硫酸除去铁片表面的铁锈:FeO+2H+═Fe2++H2O | |
| D. | 硫代硫酸钠溶液中滴加稀硫酸:2H++S2O32-═S↓+SO2↑+H2O |
8.普伐他汀是一种调节血脂的药物,其结构如图所示.下列关于普伐他汀的性质描述不正确的是( )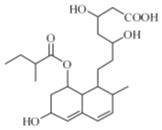

| A. | 能与FeCl3 溶液发生显色反应 | |
| B. | 能使酸性KMnO4 溶液褪色 | |
| C. | 能发生加成、取代、消去反应 | |
| D. | 1mol该物质最多可消耗4molNaOH、2molBr2 |
18.某学校化学实验室保存的硫酸试剂标签上的部分内容如图所示,则下列说法正确的是( )


| A. | 某实验需要配制460mL1.0mol/L的稀硫酸,应取该硫酸25.0mL | |
| B. | 足量铜和含2mol溶质的该硫酸在加热条件下反应,标准状况下生成气体的体积约为22.4L | |
| C. | 该硫酸与等质量的水混合所得溶液溶质的物质的量浓度小于9.2mol/L | |
| D. | 该硫酸与等体积的水混合所得溶液的溶质质量分数小于49% |
2.下列各组物质中,按单质、化合物、混合物的顺序排列正确的是( )
| A. | 稀有气体、尿素、冰水混合物 | B. | 乙醇、浓硫酸、胆矾 | ||
| C. | 金刚石、铁矿石、大理石 | D. | 水银、水蒸气、生铁 |
3.以铬酸钾为原料,电化学法制备重铬酸钾的实验装置示意图如图:下列说法不正确的是( )
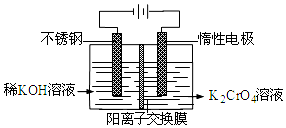

| A. | 在阴极式,发生的电极反应为:2H2O+2e-═2OH-+H2↑ | |
| B. | 在阳极室,通电后溶液逐渐由黄色变为橙色,是因为阳极区H+浓度增大,使平衡2CrO42-+2H+?Cr2O72-+H2O向右移动 | |
| C. | 该制备过程总反应的化学方程式为:4K2CrO4+4H2O$\frac{\underline{\;电解\;}}{\;}$2K2Cr2O7+4KOH+2H2↑+O2↑ | |
| D. | 铬原子的价电子排布式为3d44S2 |