题目内容
如图是有关二氧化硫性质的实验装置图,试回答下列问题:
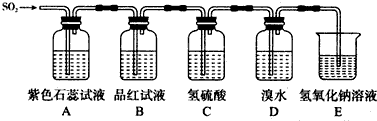
(1)A、B、C、D四个装置中发生的现象依次是 ; ; ; ;
(2)二氧化硫具有:①漂白性;②酸性氧化物性质;③还原性;④氧化性.在图中几个装置中对应表现出的性质是(填序号):
A中 ,B中 ,C中 ,D中 ;
(3)实验完毕后,将B中溶液取少量于试管中,加热,现象是 ,原因是 ;
(4)实验完毕后,取少量D中溶液于试管中,加入BaCl2溶液和稀盐酸,现象是 ;用化学方程式解释其原因 .
(5)E中发生反应的化学方程式是 .

(1)A、B、C、D四个装置中发生的现象依次是
(2)二氧化硫具有:①漂白性;②酸性氧化物性质;③还原性;④氧化性.在图中几个装置中对应表现出的性质是(填序号):
A中
(3)实验完毕后,将B中溶液取少量于试管中,加热,现象是
(4)实验完毕后,取少量D中溶液于试管中,加入BaCl2溶液和稀盐酸,现象是
(5)E中发生反应的化学方程式是
考点:探究二氧化硫与水和品红溶液的反应
专题:实验设计题
分析:二氧化硫能与水反应生成亚硫酸,亚硫酸使石蕊试液变红,体现了酸性氧化物的性质;二氧化硫具有漂白性,能使品红溶液褪色;二氧化硫能使溴水褪色,体现了还原性;二氧化硫能与氢氧化钠反应生成亚硫酸钠和水,体现酸性氧化物的性质;
根据以上知识解答(1)(2);
(3)品红溶液的漂白性不稳定,加热反应后的溶液易恢复原来颜色;
(4)二氧化硫被溴单质氧化成硫酸,硫酸与氯化钡反应生成硫酸钡沉淀,据此写出反应的化学方程式;
(5)二氧化硫有毒,能与NaOH溶液作用,吸收多余的SO2,二者反应生成亚硫酸钠和水.
根据以上知识解答(1)(2);
(3)品红溶液的漂白性不稳定,加热反应后的溶液易恢复原来颜色;
(4)二氧化硫被溴单质氧化成硫酸,硫酸与氯化钡反应生成硫酸钡沉淀,据此写出反应的化学方程式;
(5)二氧化硫有毒,能与NaOH溶液作用,吸收多余的SO2,二者反应生成亚硫酸钠和水.
解答:
解:(1)二氧化硫是酸性氧化物,能与水反应生成亚硫酸,亚硫酸使石蕊试液变红,则装置A中石蕊试液变红;
二氧化硫具有漂白性,能使品红溶液褪色,则装置B中品红溶液褪色;
二氧化硫与硫化氢反应生成浅黄色的沉淀,则装置C中出现浅黄色沉淀;
装置D中二氧化硫与溴水发生氧化还原反应,导致溴水褪色,
故答案为:变红;褪色;浅黄色沉淀;褪色;
(2)A中石蕊试液变红,原因是二氧化硫是酸性氧化物,能与水反应生成亚硫酸;
B中品红溶液褪色,因为二氧化硫具有漂白性;
C中二氧化硫能使溴水褪色,体现了还原性;
装置D溴水褪色,证明二氧化硫具有还原性,
故答案为:②;①;④;③.
(3)二氧化硫的漂白性是暂时的,加热漂白后的溶液,二氧化硫与品红生成的无色物质不稳定,加热分解导致品红溶液又恢复红色,
故答案为:溶液由无色恢复为红色;二氧化硫和有色物质生成的无色物质是不稳定的,加热后会分解;
(4)实验完毕后,取少量D中溶液于试管中,加入BaCl2溶液和稀盐酸,会观察到白色沉淀,原因为:二氧化硫与溴反应生成硫酸:SO2+Br2+2H2O═2HBr+H2SO4,稀硫酸与氯化钡反应生成硫酸钡和氯化氢:H2SO4+BaCl2═BaSO4↓+2HCl,
故答案为:产生白色沉淀;SO2+Br2+2H2O═2HBr+H2SO4、H2SO4+BaCl2═BaSO4↓+2HCl;
(5)装置E中二氧化硫与氢氧化钠溶液反应生成亚硫酸钠和水,化学方程式为:SO2+2NaOH=Na2SO3+H2O,
故答案为:SO2+2NaOH=Na2SO3+H2O.
二氧化硫具有漂白性,能使品红溶液褪色,则装置B中品红溶液褪色;
二氧化硫与硫化氢反应生成浅黄色的沉淀,则装置C中出现浅黄色沉淀;
装置D中二氧化硫与溴水发生氧化还原反应,导致溴水褪色,
故答案为:变红;褪色;浅黄色沉淀;褪色;
(2)A中石蕊试液变红,原因是二氧化硫是酸性氧化物,能与水反应生成亚硫酸;
B中品红溶液褪色,因为二氧化硫具有漂白性;
C中二氧化硫能使溴水褪色,体现了还原性;
装置D溴水褪色,证明二氧化硫具有还原性,
故答案为:②;①;④;③.
(3)二氧化硫的漂白性是暂时的,加热漂白后的溶液,二氧化硫与品红生成的无色物质不稳定,加热分解导致品红溶液又恢复红色,
故答案为:溶液由无色恢复为红色;二氧化硫和有色物质生成的无色物质是不稳定的,加热后会分解;
(4)实验完毕后,取少量D中溶液于试管中,加入BaCl2溶液和稀盐酸,会观察到白色沉淀,原因为:二氧化硫与溴反应生成硫酸:SO2+Br2+2H2O═2HBr+H2SO4,稀硫酸与氯化钡反应生成硫酸钡和氯化氢:H2SO4+BaCl2═BaSO4↓+2HCl,
故答案为:产生白色沉淀;SO2+Br2+2H2O═2HBr+H2SO4、H2SO4+BaCl2═BaSO4↓+2HCl;
(5)装置E中二氧化硫与氢氧化钠溶液反应生成亚硫酸钠和水,化学方程式为:SO2+2NaOH=Na2SO3+H2O,
故答案为:SO2+2NaOH=Na2SO3+H2O.
点评:本题考查了二氧化硫的化学性质及检验方法,题目难度中等,注意掌握二氧化硫具有的化学性质及正确的检验方法,明确二氧化硫的漂白性是暂时的,而氯水的漂白性是永久的,试题培养了学生的分析、理解能力及化学实验能力..

练习册系列答案
 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
测得VLAl2(SO4)3溶液中含Al3+mg,则该溶液中SO42-的物质的量浓度是( )
A、
| ||
B、
| ||
C、
| ||
D、
|
已知常温下Mg(OH)2的Ksp=1.8×10-11.若某氢氧化镁溶液的pH=9,则该溶液中c(Mg2+)最大为( )
| A、0.18mol/L |
| B、1.8×10-2 mol/L |
| C、1.8×10-6 mol/L |
| D、2.0×10-10mol/L |
一固体混和物,可能有氯化钙、碳酸铵、烧碱、硫酸铵,将它溶解于水得到无色澄清溶液,无其它明显现象,向溶液中加入硝酸钡溶液,产生白色沉淀,再加入硝酸,沉淀部分消失,原混和物中肯定有( )
| A、CaCl2 和(NH4)2SO4 |
| B、(NH4)2SO4 和(NH4)2CO3 |
| C、NaOH和CaCl2 |
| D、NaOH和(NH4)2SO4 |
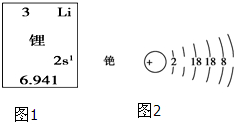 碱金属元素在科学研究与生产生活中有着非常广泛的用途.
碱金属元素在科学研究与生产生活中有着非常广泛的用途.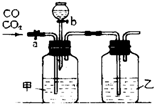 某学生用如图装置进行一氧化碳和二氧化碳混合气体的分离提纯及干燥.其中a为弹簧夹,b为分液漏斗的活塞.
某学生用如图装置进行一氧化碳和二氧化碳混合气体的分离提纯及干燥.其中a为弹簧夹,b为分液漏斗的活塞.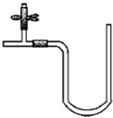 “阿波罗登月计划”总指挥韦伯在“阿波罗”登月成功后曾说:“阿波罗计划”中没有一项新发明的技术,都是现成的技术,关键在于综合.综合也是创新,例如可以用玻璃管制成的U形管、T形管、乳胶管、弹簧夹连接成如图所示的一种装置,在U型管中加入适量的红色溶液,即得简单U型气压计,我们可将它应用于多项实验,如:A.证明空气中的氧气参与氧化还原反应的实验(如铁生锈);B.溶解热效应实验(如硝酸铵溶于水);C.装置的气密性检验实验;D.检验某些气体性质的实验(如CO2,SO2、Cl2等与碱溶液的反应)等等.
“阿波罗登月计划”总指挥韦伯在“阿波罗”登月成功后曾说:“阿波罗计划”中没有一项新发明的技术,都是现成的技术,关键在于综合.综合也是创新,例如可以用玻璃管制成的U形管、T形管、乳胶管、弹簧夹连接成如图所示的一种装置,在U型管中加入适量的红色溶液,即得简单U型气压计,我们可将它应用于多项实验,如:A.证明空气中的氧气参与氧化还原反应的实验(如铁生锈);B.溶解热效应实验(如硝酸铵溶于水);C.装置的气密性检验实验;D.检验某些气体性质的实验(如CO2,SO2、Cl2等与碱溶液的反应)等等.