题目内容
仅用下表提供的玻璃仪器(非玻璃仪器任选)就能实现相应实验目的是( )
| 选项 | 实验目的 | 玻璃仪器 |
| A | 验证Na2CO3和NaHCO3的热稳定性 | 酒精灯、试管、导气管 |
| B | 用碱石灰除去氢气中混有的水蒸气并收集氢气 | 洗气瓶、导气管、集气瓶 |
| C | 用氢氧化钠和醋酸溶液测中和反应的中和热 | 烧杯、环形玻璃搅拌棒、温度计 |
| D | 分离乙醇和苯酚的混合物 | 分液漏斗、烧杯 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.碳酸氢钠不稳定,加热易分解;
B.应用固体干燥剂;
C.应该用强酸与强碱反应测中和热;
D.乙醇与苯酚互溶.
B.应用固体干燥剂;
C.应该用强酸与强碱反应测中和热;
D.乙醇与苯酚互溶.
解答:
解:A.碳酸氢钠不稳定,可在试管中加热,故A正确;
B.洗气瓶盛装液态物质,固体干燥剂碱石灰应放在干燥管中,故B错误;
C.醋酸为弱酸,电离吸热,应该用强酸与强碱反应测中和热,故C错误;
D.乙醇与苯酚互溶,不能用分液法分离,可用蒸馏的方法分离,故D错误.
故选A.
B.洗气瓶盛装液态物质,固体干燥剂碱石灰应放在干燥管中,故B错误;
C.醋酸为弱酸,电离吸热,应该用强酸与强碱反应测中和热,故C错误;
D.乙醇与苯酚互溶,不能用分液法分离,可用蒸馏的方法分离,故D错误.
故选A.
点评:本题考查较为综合,涉及物质的分离、中和热的测定等,为高考常见题型,侧重于学生的分析能力和实验能力的考查,注意实验方案的严密性和可行性的评价,难度不大.

练习册系列答案
相关题目
下列说法或有关化学用语的表达正确的是( )
| A、在基态多电子原子中,p轨道电子能量一定高于s轨道电子能量 |
B、基态Fe原子的外围电子排布图为: |
| C、因氧元素电负性比氮元素大,故氧原子第一电离能比氮原子第一电离能大 |
| D、根据原子核外电子排布的特点,Cu在周期表中属于s区元素 |
用石墨做电极电解500mLCuSO4溶液.通电一段时间后,测定两极均产生2.24L气体(标准状况下,忽略气体溶解),则CuSO4溶液的物质的量浓度为( )
| A、0.4 mol.L-1 |
| B、0.2 mol.L-1 |
| C、0.3 mol.L-1 |
| D、0.05mol.L-1 |
有关如图所示化合物的说法不正确的是( )
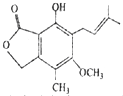

| A、该有机物的分子式为C15H18O4 |
| B、1mol该化合物最多可以与2molNaOH反应 |
| C、既可以催化加氢,又可以使酸性KMnO4溶液褪色 |
| D、既可以与FeCl3溶液发生显色反应,又可以与NaHCO3溶液反应放出CO2气体 |
下列物质既能与盐酸反应,又能与NaOH 溶液反应的是( )
| A、KHCO3 |
| B、NaOH |
| C、KAl(SO4)2 |
| D、Cu(NO3)2 |
一定条件下用甲烷可以消除氮氧化物(NOx)的污染.已知:CH4(g)+4NO(g)?2N2(g)+CO2(g)+2H2O(g)△H=-1160.0kJ?mol-1 H2O(l)=H2O(g)△H=+44.0kJ?mol-1 若取一定量的CH4和NO投入到恒容的密闭容器中,下列有关说法正确的是( )
| A、当该反应体系平均分子质量不变时,反应体系达到平衡 |
| B、当容器中每生成1 mol H2O(1)时,放出的能量为536.0kJ |
| C、升高温度,正反应速率加快,平衡常数减小 |
| D、加入高效催化剂可以一定程度上提高NO转化率 |