题目内容
下列反应最后有沉淀生成的是( )
①AlCl3溶液中加过量NaOH溶液 ②NaAlO2溶液中加过量盐酸 ③NaAlO2溶液中通入过量CO2 ④石灰水中通入过量CO2 ⑤CO2通入CaCl2溶液中 ⑥Ca(ClO)2溶液中通入过量CO2 ⑦CO2通入饱和Na2CO3溶液.
①AlCl3溶液中加过量NaOH溶液 ②NaAlO2溶液中加过量盐酸 ③NaAlO2溶液中通入过量CO2 ④石灰水中通入过量CO2 ⑤CO2通入CaCl2溶液中 ⑥Ca(ClO)2溶液中通入过量CO2 ⑦CO2通入饱和Na2CO3溶液.
| A、③⑤⑥ | B、③⑦ |
| C、⑤⑥⑦ | D、全部 |
考点:镁、铝的重要化合物
专题:几种重要的金属及其化合物
分析:①向AlCl3溶液中逐滴滴加NaOH溶液至过量,先生成氢氧化铝沉淀,后沉淀溶解;
②NaAlO2溶液中加过量盐酸,出现的现象是先沉淀后溶解;
③NaAlO2溶液中通入过量CO2 ,生成氢氧化铝沉淀;
④向澄清石灰水中通入过量的CO2,先生成碳酸钙沉淀,后沉淀溶解生成碳酸氢钙溶液;
⑤CO2与CaCl2不反应;
⑥Ca(ClO)2溶液中通入过量CO2 ,先生成碳酸钙沉淀,后沉淀溶解生成碳酸氢钙溶液;
⑦向饱和碳酸钠溶液中通入过量的CO2,析出晶体碳酸氢钠.
②NaAlO2溶液中加过量盐酸,出现的现象是先沉淀后溶解;
③NaAlO2溶液中通入过量CO2 ,生成氢氧化铝沉淀;
④向澄清石灰水中通入过量的CO2,先生成碳酸钙沉淀,后沉淀溶解生成碳酸氢钙溶液;
⑤CO2与CaCl2不反应;
⑥Ca(ClO)2溶液中通入过量CO2 ,先生成碳酸钙沉淀,后沉淀溶解生成碳酸氢钙溶液;
⑦向饱和碳酸钠溶液中通入过量的CO2,析出晶体碳酸氢钠.
解答:
解:①向AlCl3溶液中逐滴滴加NaOH溶液至过量,先生成氢氧化铝沉淀,继续滴入氢氧化钠溶液会溶解氢氧化铝沉淀,故①错误;
②NaAlO2溶液中加过量盐酸,出现的现象是先沉淀后溶解,故②错误;
③NaAlO2溶液中通入过量CO2 ,生成氢氧化铝沉淀,故③正确;
④向澄清石灰水中通入过量的CO2,先生成碳酸钙沉淀,后沉淀溶解生成碳酸氢钙溶液,反应现象是先沉淀后溶解,故④错误;
⑤CO2与CaCl2不反应,故⑤错误;
⑥Ca(ClO)2溶液中通入过量CO2 ,先生成碳酸钙沉淀,后沉淀溶解生成碳酸氢钙溶液,故⑥错误;
⑦向饱和碳酸钠溶液中通入过量的CO2,析出晶体碳酸氢钠,故⑦正确;
故选B.
②NaAlO2溶液中加过量盐酸,出现的现象是先沉淀后溶解,故②错误;
③NaAlO2溶液中通入过量CO2 ,生成氢氧化铝沉淀,故③正确;
④向澄清石灰水中通入过量的CO2,先生成碳酸钙沉淀,后沉淀溶解生成碳酸氢钙溶液,反应现象是先沉淀后溶解,故④错误;
⑤CO2与CaCl2不反应,故⑤错误;
⑥Ca(ClO)2溶液中通入过量CO2 ,先生成碳酸钙沉淀,后沉淀溶解生成碳酸氢钙溶液,故⑥错误;
⑦向饱和碳酸钠溶液中通入过量的CO2,析出晶体碳酸氢钠,故⑦正确;
故选B.
点评:本题考查了物质性质的分析应用,主要是试剂量不同产物本题的产物判断,反应现象的分析应用,掌握物质性质是解题关键,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列实验操作或记录正确的是( )
| A、用托盘天平称得2.50 g胆矾,受热充分失水后,固体质量减轻0.90 g |
| B、用100 mL量筒测得排水法收集制得的氢气体积为50.28 mL |
| C、用广泛PH试纸测得某雨水的PH为5.6 |
| D、做过焰色反应的金属丝应用稀盐酸洗,再灼烧 |
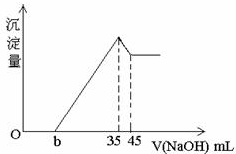 取一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,放入盛有100mlH2SO4溶液的烧杯中,充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生沉淀的量与所加NaOH溶液的体积关系如图所示.则原H2SO4物质的量溶度是( )
取一定量的铝土矿(含Al2O3、Fe2O3、SiO2)样品,放入盛有100mlH2SO4溶液的烧杯中,充分反应后过滤,向滤液中加入10mol/L的NaOH溶液,产生沉淀的量与所加NaOH溶液的体积关系如图所示.则原H2SO4物质的量溶度是( )| A、A、1mol/L |
| B、B、1.75mol/L |
| C、C、3.5mol/L |
| D、D、2mol/L |
在某一溶液中可能含有下列几种离子:K+、Fe3+、Ag+、Ba2+、NO2-、AlO2-、CO32-、SO32-、SO42-.某该溶液进行有关实验,实验步骤及结果如下:
①向溶液中加入过量稀盐酸,得到气体甲和溶液甲;
②向溶液甲中加入过量NH4HCO3溶液,得到白色沉淀乙、气体乙和溶液乙;
③向溶液乙中加入过量Ba(OH)2溶液并加热,得到白色沉淀丙、气体丙和溶液丙.
④检验气体甲、气体乙、气体丙,都只含有一种成分,而且各不相同.
下列说法正确的是( )
①向溶液中加入过量稀盐酸,得到气体甲和溶液甲;
②向溶液甲中加入过量NH4HCO3溶液,得到白色沉淀乙、气体乙和溶液乙;
③向溶液乙中加入过量Ba(OH)2溶液并加热,得到白色沉淀丙、气体丙和溶液丙.
④检验气体甲、气体乙、气体丙,都只含有一种成分,而且各不相同.
下列说法正确的是( )
| A、气体甲可能为CO2 或者SO2 |
| B、沉淀丙中一定含有BaCO3,可能含有BaSO4 |
| C、该溶液中肯定存在的离子有K+、AlO2-、SO32-、SO42-、NO2- |
| D、只根据实验①能得出溶液中一定没有Fe3+、Ag+、Ba2+,K+是否存在无法确定 |
下列各组反应中最终肯定不生成白色沉淀的是( )
| A、AlCl3溶液中加入过量氨水 |
| B、Al2(SO4)3溶液中加入过量KOH溶液 |
| C、MgCl2溶液中加入过量氨水 |
| D、澄清石灰水中通入过量CO2 |
下列各选项所描述的两个量,前者一定大于后者的是( )
| A、纯水在25℃和80℃时的pH值 |
| B、25℃时,pH=3的盐酸和AlCl3溶液中,水电离的氢离子的浓度 |
| C、耐火材料CaO和MgO的熔点 |
| D、1L pH=2的盐酸和醋酸溶液中,分别投入足量锌粒,放出H2的物质的量 |