题目内容
6.某有机物的化学式为C4H8O3,取0.1mol该有机物分别与足量的金属钠、碳酸氢钠溶液反应,生成标准状况下的气体分别为2.24L H2和2.24L CO2.则与该有机物含有相同官能团的同分异构体还有( )| A. | 3种 | B. | 5种 | C. | 4种 | D. | 6种 |
分析 0.1mol该有机物分别与足量的钠、足量的碳酸氢钠溶液反应,生成标准状况下的气体分别为2.24L即0.1molH2、2.24L即0.1molCO2,说明有机物分子中只含有1个羧基,不含有羟基,先写出丁酸的同分异构体,然后在碳和碳之间插入氧原子.
解答 解:0.1mol该有机物分别与足量的钠、足量的碳酸氢钠溶液反应,生成标准状况下的气体分别为2.24L即0.1molH2、2.24L即0.1molCO2,说明有机物分子中只含有1个羧基,不含有羟基,丁酸的同分异构体:CH3CH2CH2COOH,CH3CHCOOHCH3,则该有机物具有相同官能团的同分异构体:CH3OCH2CH2COOH,CH3CH2OCH2COOH,CH3CH2CH2OCOOH,CH3OCH(COOH)CH3,CH3CH(OCOOH)CH3,共有5种,
故选B.
点评 本题主要考查了同分异构体的书写,准确判断官能团的种类是解题的关键,难度不大.

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
14.用已知浓度的酸滴定未知浓度的碱时,会导致待测碱液的浓度偏低的操作是( )
①酸式滴定管用蒸馏水洗后,未用标准液润洗 ②碱式滴定管用蒸馏水洗后,未用待测液润洗 ③配制碱液的称量操作时固体吸潮 ④滴定前酸式滴定管尖嘴部分未充满溶液 ⑤滴定中不慎将锥形瓶内液体摇出少量于瓶外 ⑥滴定前读数正确,达到滴定终点后,俯视读数.
①酸式滴定管用蒸馏水洗后,未用标准液润洗 ②碱式滴定管用蒸馏水洗后,未用待测液润洗 ③配制碱液的称量操作时固体吸潮 ④滴定前酸式滴定管尖嘴部分未充满溶液 ⑤滴定中不慎将锥形瓶内液体摇出少量于瓶外 ⑥滴定前读数正确,达到滴定终点后,俯视读数.
| A. | ①③④ | B. | ②⑤⑥ | C. | ②③⑤⑥ | D. | ①③⑤ |
18.下列有关含硅物质的说法正确的是( )
| A. | 二氧化硅是酸性氧化物,它不溶于任何酸 | |
| B. | 高纯度的硅单质广泛用于制作光导纤维 | |
| C. | 二氧化碳通入水玻璃可以制得硅酸 | |
| D. | 水泥、玻璃、水晶饰物都是硅酸盐制品 |
15.在含有CO${\;}_{3}^{2-}$且能使酚酞试液变红的无色溶液中,能大量共存的离子组是( )
| A. | Na+、SO${\;}_{3}^{2-}$、SO${\;}_{4}^{2-}$、K+ | B. | Na+、Cu2+、Br-、Ba2+ | ||
| C. | K+、MnO${\;}_{4}^{-}$、NO${\;}_{3}^{-}$、Na+ | D. | K+、Ca2+、SO${\;}_{3}^{2-}$、Cl- |

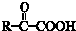 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$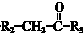
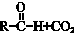 $→_{△}^{NaOH(ap)}$R1-
$→_{△}^{NaOH(ap)}$R1-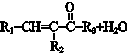
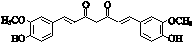 .
.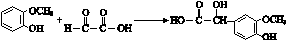 ;其反应类型是加成反应.
;其反应类型是加成反应. .
.