题目内容
一定温度下,固定容积的密闭容器中进行的可逆反应:A(g)+2B(g)?C (g)+D(g),当下列物理量不再改变时,表明反应已达平衡的是( )
| A、混合气体的密度不变 |
| B、A的消耗速率与D的生成速率相同 |
| C、单位时间内有1 mol A生成的同时,有1 mol C 消耗 |
| D、混合气体的相对分子质量不变 |
考点:化学平衡状态的判断
专题:化学平衡专题
分析:化学反应达到化学平衡状态时,正逆反应速率相等,且不等于0,各物质的浓度不再发生变化,由此衍生的一些物理量不发生变化,以此进行判断,得出正确结论.
解答:
解:A(g)+2B(g)?C (g)+D(g),
A.密度=
,总质量不变,体积不变,故混合气体的密度不再改变不能作为判断是否达到平衡状态的依据,故A错误;
B.A的消耗速率为正反应速率,D的生成速率也是正反应速率,故不能作为判断是否达到平衡状态的依据,故B错误;
C.单位时间内有1 mol A生成为逆反应,同时有1 mol C 消耗也是逆反应,故不能作为判断是否达到平衡状态的依据,故C错误;
D.平均分子量=
,总质量不变,总物质的量会变,故混合气体的相对分子质量不变可作为判断是否达到化学平衡状态的依据,故D正确;
故选D.
A.密度=
| 总质量 |
| 体积 |
B.A的消耗速率为正反应速率,D的生成速率也是正反应速率,故不能作为判断是否达到平衡状态的依据,故B错误;
C.单位时间内有1 mol A生成为逆反应,同时有1 mol C 消耗也是逆反应,故不能作为判断是否达到平衡状态的依据,故C错误;
D.平均分子量=
| 总质量 |
| 总物质的量 |
故选D.
点评:本题考查化学平衡状态的判断,题目难度不大.要注意把握平衡状态的特征.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
某烃1.68g,完全燃烧生成CO25.28g和H2O2.16g,经测定这种烃在标准状况下的密度为3.75g/L则其分子式是( )
| A、CH4 |
| B、C3H8 |
| C、C4H10 |
| D、C6H12 |
已知NO2遇水发生反应:2NO2+H2O→HNO2+HNO3.实验证明将NO2通入水会逸出NO气体,而通入NaOH溶液中则可完全被吸收,通入Na2CO3溶液中只逸出CO2.下列说法错误的是( )
| A、HNO2的酸性强于碳酸的酸性 |
| B、NO2与水的反应机理:NO2先与水发生岐化反应生成HNO2和HNO3,HNO2再分解 |
| C、HNO2非常不稳定,其分解产物为NO和H2O |
| D、NO2通入NaOH溶液中,生成的HNO2和HNO3都与NaOH发生中和反应 |
下列实验装置能达到实验目的,且实验装置无明显错误的是(夹持仪器未画出)( )
A、 甲装置用于实验室制乙烯 |
B、 乙装置用于乙酸乙酯的制备 |
C、 丙装置用于实验室制硝基苯 |
D、 丁装置可装置证明酸性:盐酸>碳酸>苯酚 |
下列有关物质的性质或应用说法正确的是( )
| A、氢氧化钠用于治疗胃溃疡病人的胃酸过多症 |
| B、金属钠具有强的还原性,可利用钠和TiCl4溶液反应制取金属Ti |
| C、糖类、油脂、蛋白质在一定条件下均可以水解 |
| D、锅炉水垢中含有的CaSO4,可先用Na2CO3溶液处理,后用酸除去 |
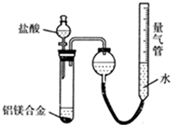 如图,某镁铝合金中,镁与铝物质的量之比为1:1,将两份质量相等的镁铝合金分别与足量的盐酸、NaOH溶液反应,生成气体的物质的量之比为( )
如图,某镁铝合金中,镁与铝物质的量之比为1:1,将两份质量相等的镁铝合金分别与足量的盐酸、NaOH溶液反应,生成气体的物质的量之比为( )| A、2:3 | B、3:2 |
| C、5:3 | D、3:5 |
下列物质的水溶液能导电,但本身是非电解质的是( )
| A、SO2 |
| B、Na |
| C、HCl |
| D、酒精 |
将铜片与浓硫酸共热,把生成的气体通入下列溶液中,能和溶质反应,最后得到无色澄清溶液的是( )
| A、亚硫酸氢钠溶液 |
| B、氢硫酸 |
| C、氢氧化钠溶液 |
| D、紫色石蕊溶液 |
某课外小组欲测定过氧化钠与碳酸钠混合物中过氧化钠的质量分数,准确称量a克样品,下列后续实验方案中,不合理的是( )
| A、隔绝空气加热,冷却后,称量剩余固体质量m1 g |
| B、与足量稀盐酸反应并蒸干,称量剩余固体质量m2 g |
| C、与足量水反应并加热,收集到标准状况下V1 L干燥气体 |
| D、与足量稀硫酸反应并加热,收集到标准状况下V2 L 干燥气体 |