题目内容
下列实验装置能达到实验目的,且实验装置无明显错误的是(夹持仪器未画出)( )
A、 甲装置用于实验室制乙烯 |
B、 乙装置用于乙酸乙酯的制备 |
C、 丙装置用于实验室制硝基苯 |
D、 丁装置可装置证明酸性:盐酸>碳酸>苯酚 |
考点:化学实验方案的评价
专题:实验评价题
分析:A.乙醇在浓硫酸作用下加热到170°C,生成乙烯和水;
B.导气管不能插在碳酸钠溶液中;
C.实验室制硝基苯在50-60℃下发生反应;
D.发生强酸制取弱酸的反应,但盐酸易挥发,干扰碳酸与苯酚酸性的比较.
B.导气管不能插在碳酸钠溶液中;
C.实验室制硝基苯在50-60℃下发生反应;
D.发生强酸制取弱酸的反应,但盐酸易挥发,干扰碳酸与苯酚酸性的比较.
解答:
解:A.实验室制乙烯的条件是迅速加热到170°C,温度计应测定反应液的温度,故A错误;
B.乙酸和乙醇在浓硫酸加热条件下生成乙酸乙酯和水,产物中混有乙酸和乙醇,导气管不能插在碳酸钠溶液中,防止倒吸,故B正确;
C.实验室制硝基苯,需要用水浴加热50-60℃下发生反应,不是100度,故C错误;
D.发生强酸制取弱酸的反应,但盐酸易挥发,干扰碳酸与苯酚酸性的比较,装置只能说明酸性盐酸>碳酸,故D错误.
故选B.
B.乙酸和乙醇在浓硫酸加热条件下生成乙酸乙酯和水,产物中混有乙酸和乙醇,导气管不能插在碳酸钠溶液中,防止倒吸,故B正确;
C.实验室制硝基苯,需要用水浴加热50-60℃下发生反应,不是100度,故C错误;
D.发生强酸制取弱酸的反应,但盐酸易挥发,干扰碳酸与苯酚酸性的比较,装置只能说明酸性盐酸>碳酸,故D错误.
故选B.
点评:本题考查常见化学实验装置的使用,位置制备的实验装置和使用方法,注意问题,难度不大,注意蒸馏装置、制乙烯装置中的温度计的正确使用,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
用氯气跟单质化合不能制取的物质是( )
| A、KCl |
| B、FeCl2 |
| C、FeCl3 |
| D、CuCl2 |
在NO2被水吸收的反应中,氧化产物与还原产物的物质的量之比为( )
| A、3:1 | B、1:3 |
| C、1:2 | D、2:1 |
已知某条件下,合成氨反应的数据如下:
N2(g)+3H2(g)
2NH3(g)
起始浓度/mol.L-1 1.0 3.0 0.2
2s末浓度/mol.L-1 0.6 1.8 1.0
4s末浓度/mol.L-1 0.4 1.2 1.4
当用氨气浓度的增加来表示该反应的速率时,下列说法中错误的是( )
N2(g)+3H2(g)
| ||
| 高温高压 |
起始浓度/mol.L-1 1.0 3.0 0.2
2s末浓度/mol.L-1 0.6 1.8 1.0
4s末浓度/mol.L-1 0.4 1.2 1.4
当用氨气浓度的增加来表示该反应的速率时,下列说法中错误的是( )
| A、2s末氨气的反应速率为0.4 mol?L-1?s-1 |
| B、前2s时间内氨气的平均反应速率为0.4 mol?L-1?s-1 |
| C、前4s时间内氨气的平均反应速率为0.3 mol?L-1?s-1 |
| D、2~4s时间内氨气的平均反应速率为0.2 mol?L-1?s-1 |
下列气体实验中,正确的是( )
A、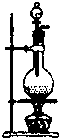 铜和稀硝酸制一氧化氮气体 |
B、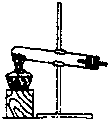 加热Cu(NO3)2(s)获取NO2(g) |
C、 浓硫酸滴入浓盐酸中制HCl |
D、 硫化氢气体的干燥与收集 |
一定温度下,固定容积的密闭容器中进行的可逆反应:A(g)+2B(g)?C (g)+D(g),当下列物理量不再改变时,表明反应已达平衡的是( )
| A、混合气体的密度不变 |
| B、A的消耗速率与D的生成速率相同 |
| C、单位时间内有1 mol A生成的同时,有1 mol C 消耗 |
| D、混合气体的相对分子质量不变 |
某瓶中的混合气体呈棕红色,加足量水盖严后震荡气体变为无色,溶液为橙色,开盖后气体又呈棕红色,则原来瓶中的气体不可能是( )
| A、NO2、N2、Br2蒸气 |
| B、NO2、NO、Br2蒸气 |
| C、NO2、CO2、Br2蒸气 |
| D、NO2、NO、N2 |
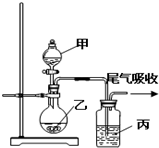 用下图所示装置进行实验中,将甲中的液体滴加到乙中,均有气泡出现,根据乙、丙装置中出现的现象得出的结论且正确的是( )
用下图所示装置进行实验中,将甲中的液体滴加到乙中,均有气泡出现,根据乙、丙装置中出现的现象得出的结论且正确的是( )