题目内容
8.在一定容积密闭容器中加入2mol A和3mol B,在一定温度下发生反应:A(g)+B(g)?C(g)+D(g),下列可作判断反应是否达到平衡的依据的是( )| A. | 气体的密度是否变化 | |
| B. | 容器内的压强是否变化 | |
| C. | 容器中A的浓度是否变化 | |
| D. | 容器中C、D的物质的量之比是否变化 |
分析 当正逆反应速率相等时可逆反应达到平衡状态,反应体系中各物质的物质的量、物质的量浓度、百分含量以及由此引起的一系列物理量不变,据此分析解答.
解答 解:A.根据质量守恒定律及物质状态知,反应前后气体总质量不变、容器体积不变,所以气体密度始终不变,不能据此平衡平衡状态,故A不选;
B.反应前后气体计量数之和不变,所以无论是否达到平衡状态,气体压强始终不变,不能据此判断平衡状态,故B不选;
C.随着反应减小,A的浓度逐渐减小,当A的浓度不变时,其正逆反应速率相等,该反应达到平衡状态,所以可以据此判断平衡状态,故C选;
D.C、D的计量数相等且都是生成物,开始时容器中都不存在C、D物质,所以容器中C、D的物质的量之比始终都是1:1,不能据此判断平衡状态,故D不选;
故选C.
点评 本题考查化学平衡状态判断,为高频考点,只有反应前后改变的物理量不变时可逆反应才能达到平衡状态,难点是判断平衡状态依据的选取,易错选项是A.

练习册系列答案
相关题目
19.将标准状况下1.12L CO2通入含有2g NaOH的水溶液中,完全反应并得到2L溶液,则对于该溶液表述正确的是( )
| A. | CO2和NaOH完全反应生成碳酸氢钠 | |
| B. | 反应所得溶液呈酸性 | |
| C. | HCO3-的电离程度大于HCO3-的水解程度 | |
| D. | 存在的平衡体系只有:HCO3-+H2O?H2CO3+OH-,HCO3-?H++CO32- |
18.通常状况下,单斜硫和正交硫是硫的两种固态的同素异形体.已知热化学方程式:
①S(s,单斜)+O2(g)→SO2 (g)+297.16kJ
②S(s,正交)+O2(g)→SO2 (g)+296.83kJ
下列说法错误的是( )
①S(s,单斜)+O2(g)→SO2 (g)+297.16kJ
②S(s,正交)+O2(g)→SO2 (g)+296.83kJ
下列说法错误的是( )
| A. | 单斜硫比正交硫稳定 | |
| B. | 单斜硫转化为正交硫需要放出热量 | |
| C. | 单斜硫升华为气态时要吸收热量 | |
| D. | 将同态的硫单质气化或液化能提高它们的燃烧效率 |
 ,它的分子式是C6H8O6.在维生素C溶液中滴入紫色石蕊试液,溶液颜色变红,说明维生素C溶液具有酸性.
,它的分子式是C6H8O6.在维生素C溶液中滴入紫色石蕊试液,溶液颜色变红,说明维生素C溶液具有酸性. 的合成路线如下:
的合成路线如下:
 中含有的官能团名称为硝基,氟原子.
中含有的官能团名称为硝基,氟原子. 一定条件下形成聚合物的结构简式为
一定条件下形成聚合物的结构简式为 .
.
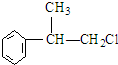 或
或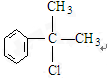 ;
;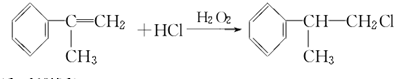 ;
;