题目内容
13.将0.6molA和0.5molB 充入0.4L密闭容器中发生2A(g)+B(g)?mD (g)+E(g),5min 后达到化学平衡,此时测得D为0.2mol.又知5min内用E表示的平均反应速率为0.1mol•L-1•min-1,计算:(1)m的值
(2)平衡时B的转化率
(3)起始与平衡时密闭容器中的压强之比.
分析 5min 后达到化学平衡,此时测得D为0.2mol,则v(D)=$\frac{\frac{0.2mol}{0.4L}}{5min}$=0.1mol•L-1•min-1,又知5min内用E表示的平均反应速率为0.1mol•L-1•min-1,反应速率之比等于化学计量数之比,可知m=1,则
2A(g)+B(g)?D (g)+E(g)
开始 0.6 0.5 0 0
转化 0.4 0.2 0.2 0.2
平衡 0.2 0.3 0.2 0.2
结合转化率=$\frac{转化的量}{开始的量}$、物质的量比等于压强的比来解答.
解答 解:5min 后达到化学平衡,此时测得D为0.2mol,则v(D)=$\frac{\frac{0.2mol}{0.4L}}{5min}$=0.1mol•L-1•min-1,又知5min内用E表示的平均反应速率为0.1mol•L-1•min-1,反应速率之比等于化学计量数之比,可知m=1,则
2A(g)+B(g)?D (g)+E(g)
开始 0.6 0.5 0 0
转化 0.4 0.2 0.2 0.2
平衡 0.2 0.3 0.2 0.2
(1)由上述分析可知,计量数m=1,
答:m的值为1;
(2)B的转化率为$\frac{0.2mol}{0.5mol}$×100%=40%,
答:平衡时B的转化率为40%;
(3)平衡时混合物总物质的量为0.2mol+0.3mol+0.2mol+0.2mol=0.9mol,起始时混合物总物质的量为0.6mol+0.5mol=1.lmol,由于容器的容积不变,所以气体的物质的量的比等于容器内气体的压强之比,故起始与平衡时密闭容器中的压强之比为11:9,
答:起始与平衡时密闭容器中的压强之比为11:9.
点评 本题考查化学平衡的计算,为高频考点,把握化学平衡三段法、转化率及压强比的计算为解答的关键,侧重分析与计算能力的考查,注意物质的量比与压强比的关系,题目难度不大.

| A. | 颜色变浅 | B. | 逐渐变深绿 | C. | 没有改变 | D. | 变棕黄色 |
| A. | 9种 | B. | 12种 | C. | 13种 | D. | 14种 |
| A. | 含有少量碳酸氢钙和氯化钙的水是永久硬水 | |
| B. | 明矾有净水作用,所以用明矾处理硬水,可以使硬水软化 | |
| C. | 用离子交换剂处理硬水,可使硬水软化 | |
| D. | 只具有永久硬度的水经加热煮沸后,可变成软水 |
| A. | 遇氯化氢产生白烟 | B. | 能使湿润的蓝色石蕊试纸变红 | ||
| C. | 刺激性气味、密度比空气小 | D. | 其水溶液能使酚酞溶液变红 |
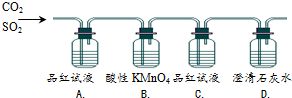
| 编号 | 实验现象 | 实验目的 |
| A. | 品红褪色 | 证明混合气体中有SO2 |
| B. | KMnO4褪色 | 证明SO2有还原性 |
| C. | 品红不褪色 | 证明进入C的气体中没有SO2 |
| D. | 石灰水变浑浊 | 证明混合气体中有CO2 |
| A. | A | B. | B | C. | C | D. | D |