题目内容
3.用图装置验证浓硫酸和木炭反应的产物中有SO2和CO2,对有关实验现象和实验目的描述中错误的是( )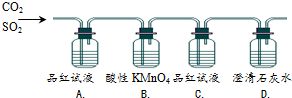
| 编号 | 实验现象 | 实验目的 |
| A. | 品红褪色 | 证明混合气体中有SO2 |
| B. | KMnO4褪色 | 证明SO2有还原性 |
| C. | 品红不褪色 | 证明进入C的气体中没有SO2 |
| D. | 石灰水变浑浊 | 证明混合气体中有CO2 |
| A. | A | B. | B | C. | C | D. | D |
分析 二氧化硫能和品红溶液反应生成无色物质而体现漂白性;
酸性高锰酸钾溶液具有强氧化性,能氧化还原性物质;
二氧化碳和二氧化硫都能使澄清石灰水变浑浊.
解答 解:A.二氧化硫能和品红溶液反应生成无色物质而体现漂白性,二氧化碳没有漂白性,所以如果A中溶液褪色,能证明含有二氧化硫,故A不选;
B.酸性高锰酸钾溶液具有强氧化性,能氧化还原性物质,二氧化碳没有还原性,所以二氧化碳不能使酸性高锰酸钾溶液褪色,通入的气体能使酸性高锰酸钾溶液褪色能证明二氧化硫的还原性,但B装置目的是除去二氧化硫,故B选;
C.二氧化硫能使品红溶液褪色,但进入C装置的溶液不褪色,证明通入C装置的气体中不含二氧化硫,故C不选;
D.二氧化碳和二氧化硫都能使澄清石灰水变浑浊,通过C知,通入D的气体中不含二氧化硫,D中溶液变浑浊,说明该气体是二氧化碳,实验现象和目的正确,故D不选;
故选B.
点评 本题考查化学实验方案评价,为高频考点,明确实验原理、物质性质是解本题关键,侧重考查学生实验操作、实验观察分析及判断能力,注意B的实验目的,为易错点.

练习册系列答案
相关题目
11.下图所示实验基本操作正确的是( )
| A. |  | B. |  | C. | 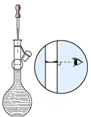 | D. |  |
12.化学深入我们生活,下列说法正确的是( )
| A. | PX 项目的主要产品对二甲苯属于饱和烃 | |
| B. | 食用花生油和鸡蛋清都能发生水解反应 | |
| C. | 包装用材料聚乙烯和聚氯乙烯都属于烃 | |
| D. | 保护加酶洗衣粉的洗涤效果,应用沸水溶解洗衣粉 |
13.下列相关实验不能达到预期目的是( )
| 相关实验 | 预期目的 | |
| A | 向少量燃尽火柴头的浸泡液中滴加稀硫酸,AgNO3 | 验证火柴头含有氯元素 |
| B | 向两支装有等体积,等浓度的H2O2溶液试管中分别加入1mol等浓度的FeCl3溶液、CuSO4溶液 | 催化效果:Fe3+>Cu2+ |
| C | 向待测溶液中加NaOH溶液后加热,产生使湿润的红色石蕊试纸变蓝的气体 | 证明原溶液中含有NH4+ |
| D | 向等浓度的NaCl、KI混合液中逐滴加入AgNO3溶液先出现黄色沉淀 | K(sp),AgCl>AgI |
| A. | A | B. | B | C. | C | D. | D |

 .
.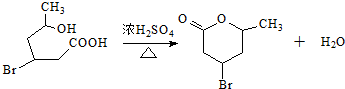 .
. (2-甲基-1,3-丁二烯)发生类似①的反应,得到有机物VI和VII,结构简式分别是为HCHO、CH3COCHO,它们物质的量之比是2:1.
(2-甲基-1,3-丁二烯)发生类似①的反应,得到有机物VI和VII,结构简式分别是为HCHO、CH3COCHO,它们物质的量之比是2:1.