题目内容
体积相同的盐酸和醋酸两种溶液,n(Cl-)=n(CH3COO-)=0.01mol,下列叙述错误的是( )
| A.它们与NaOH完全中和时,醋酸所消耗的NaOH多 |
| B.它们分别与足量CaCO3反应时,放出的CO2一样多 |
| C.两种溶液的pH相同 |
| D.分别用水稀释相同倍数后,n(Cl-)<n(CH3COO-) |
体积相同的盐酸和醋酸两种溶液,溶液中n(Cl-)=N(CH3COO-),所以溶液中氢离子浓度相同,但因醋酸为弱酸,则醋酸的浓度大,等体积时醋酸的物质的量多,
A、醋酸存在电离平衡,平衡状态下氢离子浓度和盐酸溶液中氢离子浓度相同,与碱反应时醋酸消耗氢氧化钠多;故A正确;
B、醋酸存在电离平衡,平衡状态下氢离子浓度和盐酸溶液中氢离子浓度相同,和足量碳酸钙反应,醋酸电离平衡正向进行又电离出氢离子进行溶解碳酸钙;放出的CO2不一样多,醋酸生成二氧化碳多,故B错误;
C、盐酸和醋酸是一元酸,溶液中n(Cl-)=n(CH3COO-),所以溶液中氢离子浓度相同,PH相同;故C正确;
D、溶液稀释相同倍数,弱酸存在电离平衡,稀释促进电离,离子浓度变化小;所以n(Cl-)<n(CH3COO-),故D正确;
故选B.
A、醋酸存在电离平衡,平衡状态下氢离子浓度和盐酸溶液中氢离子浓度相同,与碱反应时醋酸消耗氢氧化钠多;故A正确;
B、醋酸存在电离平衡,平衡状态下氢离子浓度和盐酸溶液中氢离子浓度相同,和足量碳酸钙反应,醋酸电离平衡正向进行又电离出氢离子进行溶解碳酸钙;放出的CO2不一样多,醋酸生成二氧化碳多,故B错误;
C、盐酸和醋酸是一元酸,溶液中n(Cl-)=n(CH3COO-),所以溶液中氢离子浓度相同,PH相同;故C正确;
D、溶液稀释相同倍数,弱酸存在电离平衡,稀释促进电离,离子浓度变化小;所以n(Cl-)<n(CH3COO-),故D正确;
故选B.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列图示与对应的叙述相符的是( )
A、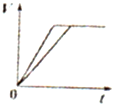 表示物质的量之比为2:3的镁和铝分别与过量稀硫酸反应时,产生气体的体积(V)与时间(t)的关系 | B、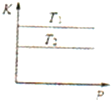 表示2SO2(g)+O2(g)?2SO3(g)(△H<0)的平衡常数K与压强P的关系且T1<T2 | C、 表示用0.1mol-L-1NaOH溶液分别滴定浓度均为0.1mol?L-1体积相同的盐酸和醋酸,其中的虚线是滴定醋酸的曲线 | D、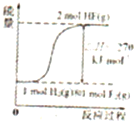 表示在相同条件下1 mol H2(g)与1 mol F2(g)反应生成2 mol HF(g)时,放出的热童为270kJ |