题目内容
各物质之间的转化关系如图,部分生成物省略.C、D是由X、Y、Z中两种元素组成的化合物,X、Y、Z的原子序数依次增大,在周期表中X的原子半径最小,Y、Z原子最外层电子数之和为10.D为无色非可燃性气体,G为黄绿色单质气体,J、M为金属,I有漂白作用,反应①常用于制作印刷电路板.

请回答下列问题:
(1)写出B的化学式 ,I的电子式 ;
(2)M的硝酸盐水溶液显酸性,用离子方程式解释原因 ;
(3)写出反应②的化学方程式(有机物用结构简式表示) ;
(4)写出M溶于稀H2SO4和H2O2混合液的化学方程式 ;
(5)G单质所含元素的最高价氧化物为无色液体,0.25mol该物质与一定量水混合得到一种稀溶液,并放出Q KJ的热量.写出该反应的热化学方程式 .

请回答下列问题:
(1)写出B的化学式
(2)M的硝酸盐水溶液显酸性,用离子方程式解释原因
(3)写出反应②的化学方程式(有机物用结构简式表示)
(4)写出M溶于稀H2SO4和H2O2混合液的化学方程式
(5)G单质所含元素的最高价氧化物为无色液体,0.25mol该物质与一定量水混合得到一种稀溶液,并放出Q KJ的热量.写出该反应的热化学方程式
考点:无机物的推断
专题:推断题
分析:X在周期表中的原子半径最小,则X为H元素;Y、Z原子最外层电子数之和为10,“X、Y、Z的原子序数依次增大”,C、D是由X、Y、Z中两种元素组成的化合物,D为无色非可燃性气体,考虑Y、Z为C、O两种元素,则D为CO2,C为H2O.G为黄绿色单质气体,则G应为Cl2,由C+G→H+I,可知生成HCl和HClO,I有漂白作用,应为HClO,则H为HCl,浅绿色、棕黄色溶液为Fe2+和Fe3+,可知J为Fe,K为FeCl2,L为FeCl3,反应①用于制作印刷电路板为FeCl3和Cu,则M为Cu,B为CuCl2,E能与葡萄糖反应,应为Cu(OH)2,F为Cu2O,从A+H(HCl)=B(CuCl2)+C(H2O)+D(CO2)可知,A是含有Cu2+的碳酸盐,应为CuCO3或Cu2(OH)2CO3,据此解答.
解答:
解:X在周期表中的原子半径最小,则X为H元素;Y、Z原子最外层电子数之和为10,“X、Y、Z的原子序数依次增大”,C、D是由X、Y、Z中两种元素组成的化合物,D为无色非可燃性气体,考虑Y、Z为C、O两种元素,则D为CO2,C为H2O.G为黄绿色单质气体,则G应为Cl2,由C+G→H+I,可知生成HCl和HClO,I有漂白作用,应为HClO,则H为HCl,浅绿色、棕黄色溶液为Fe2+和Fe3+,可知J为Fe,K为FeCl2,L为FeCl3,反应①用于制作印刷电路板为FeCl3和Cu,则M为Cu,B为CuCl2,E能与葡萄糖反应,应为Cu(OH)2,F为Cu2O,从A+H(HCl)=B(CuCl2)+C(H2O)+D(CO2)可知,A是含有Cu2+的碳酸盐,应为CuCO3或Cu2(OH)2CO3,
(1)由以上分析可知,B是CuCl2,I为HClO,电子式为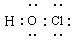 ,故答案为:CuCl2;
,故答案为:CuCl2;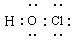 ;
;
(2)Cu(NO3)2溶液中铜离子水解,溶液呈酸性,离子方程式为:Cu2++2H2O?Cu(OH)2+2H+,故答案为:Cu2++2H2O?Cu(OH)2+2H+;
(3)葡萄糖和氢氧化铜浊液在加热条件下反应的方程式为:CH2OH(CHOH)4CHO+2Cu(OH)2
CH2OH(CHOH)4COOH+Cu2O↓+2H2O,
故答案为:CH2OH(CHOH)4CHO+2Cu(OH)2
CH2OH(CHOH)4COOH+Cu2O↓+2H2O;
(4)Cu溶于稀H2SO4和H2O2混合液的化学方程式为:Cu+H2SO4+H2O2=CuSO4+2H2O,故答案为:Cu+H2SO4+H2O2=CuSO4+2H2O;
(5)G为Cl2,最高价氧化物为Cl2O7,0.25mol该物质与一定量水混合得到HClO4,放出Q KJ的热量,该反应的热化学方程式为:Cl2O7(l)+H2O(l)=2HClO4(aq)△H=-4Q KJ/mol,故答案为:Cl2O7(l)+H2O(l)=2HClO4(aq)△H=-4Q KJ/mol.
(1)由以上分析可知,B是CuCl2,I为HClO,电子式为
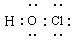 ,故答案为:CuCl2;
,故答案为:CuCl2;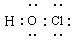 ;
;(2)Cu(NO3)2溶液中铜离子水解,溶液呈酸性,离子方程式为:Cu2++2H2O?Cu(OH)2+2H+,故答案为:Cu2++2H2O?Cu(OH)2+2H+;
(3)葡萄糖和氢氧化铜浊液在加热条件下反应的方程式为:CH2OH(CHOH)4CHO+2Cu(OH)2
| △ |
故答案为:CH2OH(CHOH)4CHO+2Cu(OH)2
| △ |
(4)Cu溶于稀H2SO4和H2O2混合液的化学方程式为:Cu+H2SO4+H2O2=CuSO4+2H2O,故答案为:Cu+H2SO4+H2O2=CuSO4+2H2O;
(5)G为Cl2,最高价氧化物为Cl2O7,0.25mol该物质与一定量水混合得到HClO4,放出Q KJ的热量,该反应的热化学方程式为:Cl2O7(l)+H2O(l)=2HClO4(aq)△H=-4Q KJ/mol,故答案为:Cl2O7(l)+H2O(l)=2HClO4(aq)△H=-4Q KJ/mol.
点评:本题综合考查无机框图物质的推断,侧重考查Cu、Fe、Cl2及化合物知识,题目渗透有机物知识,注意根据物质的颜色、性质进行推断,需要学生熟练掌握元素化合物知识,题目难度较大.

练习册系列答案
相关题目
有一混合溶液,其中含有Fe2+、Cl-、Br-、I-,其中Cl-、Br-、I-的个数比为2:3:4,向该溶液中通入Cl2,使溶液中Cl-和Br-的个数比为3:1,则通入Cl2的物质的量与溶液中剩余的Fe2+的物质的量之比为:( )(已知还原性I->Fe2+>Br->Cl-水电离产生的H+和OH-忽略不计)
| A、7:1 | B、7:2 |
| C、7:3 | D、7:4 |
下列反应属于加成反应的是( )
| A、甲烷与氯气的混合气体在光照条件下的反应 |
| B、丙烯和氯气在一定条件下生成ClCH2CH=CH2的反应 |
| C、乙烯使酸性高锰酸钾溶液褪色的反应 |
| D、乙烯与溴水的反应 |
从植物花汁中提取的一种有机物,可简化表示为HIn,在水溶液中因存在下列电离平衡,故可用做酸、碱指示剂:HIn(红色溶液)?H+(溶液)+In-(黄色溶液),在上述溶液中加入下列物质,最终能使指示剂显黄色的是( )
| A、盐酸 |
| B、NaHCO3溶液 |
| C、NaHSO4溶液 |
| D、Na2SO4固体 |
常温下,0.1mol?L-1某一元酸(HA)溶液中
=1×10-8,下列叙述正确的是( )
| c(OH-) |
| c(H+) |
| A、该溶液中由水电离出的c(H+)=1×10-1mol?L-1 |
| B、浓度均为0.1mol/L的HA和NaA溶液等体积混合后,若溶液呈酸性,则c(A-)>c(HA)>c(Na+)>c(H+)>c(OH-) |
| C、0.1 mol?L-1HA溶液与0.05 mol?L-1NaOH溶液等体积混合后所得溶液中 c(A-)+c(HA)=c(Na+) |
| D、0.1 mol?L-1HA溶液与0.05 mol?L-1NaOH溶液等体积混合后所得溶液中 2c(H+)+c(HA)=c(A-)+2c(OH-) |
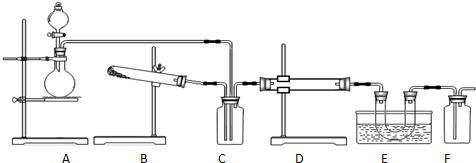
 A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件未标出),其中A、D是中学化学中常见的单质.
A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件未标出),其中A、D是中学化学中常见的单质.