题目内容
(1)下列3种不同粒子
H、
H、
H表示 种元素, 种核素,
H、
H、
H互称为 .
(2)下列各组物质中,互称为同分异构体的是
A.水与冰
B.O2与O3
C. 与
与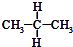
D.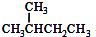 与
与
(3)写出电子式:①OH-: ;②N2: ;③K2O: ;④CO2: .
1 1 |
2 1 |
3 1 |
1 1 |
2 1 |
3 1 |
(2)下列各组物质中,互称为同分异构体的是
A.水与冰
B.O2与O3
C.
 与
与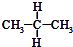
D.
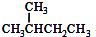 与
与
(3)写出电子式:①OH-:
考点:核素,电子式,同分异构现象和同分异构体
专题:同系物和同分异构体
分析:(1)根据元素的种类由质子数决定分析,根据质子数、中子数和核数、同位素的概念判断;
(2)具有相同分子式而结构不同的化合物互为同分异构体;
(3)①氢氧根离子是由氧原子和氢原子以共价键组成的原子团,带一个负电荷;
②氮气中存在3对共用电子对,氮原子最外层达到8个电子;
③氧化钾为离子化合物,必须标出阴阳离子的电子式;
④二氧化碳中存在两个碳氧键,C、O原子最外层都达到最外层8个电子.
(2)具有相同分子式而结构不同的化合物互为同分异构体;
(3)①氢氧根离子是由氧原子和氢原子以共价键组成的原子团,带一个负电荷;
②氮气中存在3对共用电子对,氮原子最外层达到8个电子;
③氧化钾为离子化合物,必须标出阴阳离子的电子式;
④二氧化碳中存在两个碳氧键,C、O原子最外层都达到最外层8个电子.
解答:
解:(1)元素就是具有相同的核电荷数(即核内质子数)的一类原子的总称,不同种元素最本质的区别是质子数不同,元素的种类由质子数决定,11H、12H、13H的质子数都是1,所以3种不同粒子
H、
H、
H表示同一种元素氢元素;
核素是指具有一定数目质子和一定数目中子的一种原子;11H、12H、13H的质子数都是1,中子数分别为0、1、2,属于三种核数;
具有相同质子数,不同中子数同一元素的不同核素互为同位素;11H、12H、13H的质子数都是1,中子数分别为0、1、2,属于同位素;
故答案为:1;3;同位素;
(2)具有相同分子式而结构不同的化合物互为同分异构体.
A、水与冰的化学成分相同,为同一种物质,故A不选;
B、O2与O3是由氧元素组成的结构不同的单质,互为同素异形体,故B不选;
C、 与
与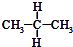 均为正丙烷,为同一种物质,故C不选;
均为正丙烷,为同一种物质,故C不选;
D、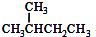 与
与 的分子式相同,结构不同的烷烃,互为同分异构体,故D选;
的分子式相同,结构不同的烷烃,互为同分异构体,故D选;
故答案为:D;
(3)①氢氧根离子是由氧原子和氢原子以共价键组成的原子团,带一个负电荷,电子式为 ,
,
故答案为: ;
;
②氮气中存在3对共用电子对,氮原子最外层达到8个电子,电子式为 ,
,
故答案为: ;
;
③氧化钾是由钾离子和氧离子组成的离子化合物,把氧离子写在中间,电子式为 ,
,
故答案为: ;
;
④二氧化碳中存在两个碳氧键,C、O原子最外层都达到最外层8个电子,电子式为 ,
,
故答案为: .
.
1 1 |
2 1 |
3 1 |
核素是指具有一定数目质子和一定数目中子的一种原子;11H、12H、13H的质子数都是1,中子数分别为0、1、2,属于三种核数;
具有相同质子数,不同中子数同一元素的不同核素互为同位素;11H、12H、13H的质子数都是1,中子数分别为0、1、2,属于同位素;
故答案为:1;3;同位素;
(2)具有相同分子式而结构不同的化合物互为同分异构体.
A、水与冰的化学成分相同,为同一种物质,故A不选;
B、O2与O3是由氧元素组成的结构不同的单质,互为同素异形体,故B不选;
C、
 与
与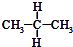 均为正丙烷,为同一种物质,故C不选;
均为正丙烷,为同一种物质,故C不选;D、
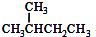 与
与 的分子式相同,结构不同的烷烃,互为同分异构体,故D选;
的分子式相同,结构不同的烷烃,互为同分异构体,故D选;故答案为:D;
(3)①氢氧根离子是由氧原子和氢原子以共价键组成的原子团,带一个负电荷,电子式为
 ,
,故答案为:
 ;
;②氮气中存在3对共用电子对,氮原子最外层达到8个电子,电子式为
 ,
,故答案为:
 ;
;③氧化钾是由钾离子和氧离子组成的离子化合物,把氧离子写在中间,电子式为
 ,
,故答案为:
 ;
;④二氧化碳中存在两个碳氧键,C、O原子最外层都达到最外层8个电子,电子式为
 ,
,故答案为:
 .
.
点评:本题考查了元素、核素、同素异形体、同分异构体等概念、电子式的书写,题目难度中等,注意掌握电子式的概念及书写原则,明确离子化合物与共价化合物的电子式表示方法及区别.

练习册系列答案
相关题目
用石油和煤可以得到有机化工生产中需要的众多原料,例如由石油得到的乙烯和煤得到的苯制聚苯乙烯.生产过程如下:

下列说法不正确的是( )

下列说法不正确的是( )
| A、通过裂解可以从石油中获得更多的乙烯 |
| B、把煤干馏不能直接得到苯 |
| C、制聚苯乙烯的反应①为加成反应,③为缩聚反应 |
| D、反应①②③的原子利用率都达到了100% |
我国知名企业比亚迪公司开发了具有多项专利的锂钒氧化物二次电池,其成本较低,对环境无污染,能量密度远远高于其他材料电池,电池总反应为V2O5+xLi
LixV2O5.下列说法中正确的是( )
| 放电 |
| 充电 |
| A、电池在放电时,Li+向负极移动 |
| B、锂在放电时做正极,充电时为阳极 |
| C、该电池充电时阳极的反映为LixV2O5-xe-═V2O5+xLi+ |
| D、V2O5只是锂发生反应的载体,不参与电池反应 |
SF6是一种优良的绝缘气体,分子结构中存在S-F键.已知S8(s)的分子结构模型(如图),断裂1mol S-S、1molF-F、1mol S-F键需吸收的能量分别为280kJ、160kJ、330kJ.则
S8(s)+3F2(g)═SF6(g)的反应热△H为( )
| 1 |
| 8 |

| A、-1780kJ?mol-1 |
| B、-1220kJ?mol-1 |
| C、-450 kJ?mol-1 |
| D、+430kJ?mol-1 |


