题目内容
(1)相对分子质量为58的烷烃其分子式是 ;
(2)1mol该烷烃完全燃烧消耗标准状况下的氧气体积为 L;
(3)它可能的结构简式是 , ;
(4)另有相对分子质量为58的含氧有机物,其可能的结构简式为 .(写一种即可)
(2)1mol该烷烃完全燃烧消耗标准状况下的氧气体积为
(3)它可能的结构简式是
(4)另有相对分子质量为58的含氧有机物,其可能的结构简式为
考点:烷烃及其命名,有机物实验式和分子式的确定
专题:有机化学基础
分析:(1)设烷烃的分子式为CnH2n+2,根据相对分子质量为58,列出方程式进行计算n值;
(2)1mol丁烷完全燃烧消耗的氧气的物质的量为(4+
)mol,带入V=nVm计算体积;
(3)丁烷有两种同分异构体,主链有4个碳原子的正丁烷CH3CH2CH2CH3,主链有3个碳原子的异丁烷:CH3CH(CH3)CH3;
(4)当该含氧有机物含有1个氧原子时,则剩余的式量是42,利用余商法计算确定可能的分子式,写出可能的结构简式.
(2)1mol丁烷完全燃烧消耗的氧气的物质的量为(4+
| 10 |
| 4 |
(3)丁烷有两种同分异构体,主链有4个碳原子的正丁烷CH3CH2CH2CH3,主链有3个碳原子的异丁烷:CH3CH(CH3)CH3;
(4)当该含氧有机物含有1个氧原子时,则剩余的式量是42,利用余商法计算确定可能的分子式,写出可能的结构简式.
解答:
解:(1)设烷烃的分子式为CnH2n+2,则
14n+2=58,解得n=4,
所以该烷烃的分子式为C4H10,
故答案为:C4H10;
(2)1molC4H10完全燃烧消耗的氧气的物质的量为(4+
)mol=6.5mol,在标准状况下的体积V=6.5mol×22.4L/mol=145.6L,
故答案为:145.6;
(3)丁烷有两种同分异构体,主链有4个碳原子的正丁烷CH3CH2CH2CH3,主链有3个碳原子的异丁烷:CH3CH(CH3)2,
故答案为:CH3CH2CH2CH3;CH3CH(CH3)2;
(4)当该含氧有机物含有1个氧原子时,则剩余的式量是42,
=3,剩余部分组成为C3H6,该有机物可能的分子式为C3H6O,可能的结构简式为CH3COCH3或CH2=CH-CH2OH,
故答案为:CH2=CH-CH2OH( 或CH3COCH3).
14n+2=58,解得n=4,
所以该烷烃的分子式为C4H10,
故答案为:C4H10;
(2)1molC4H10完全燃烧消耗的氧气的物质的量为(4+
| 10 |
| 4 |
故答案为:145.6;
(3)丁烷有两种同分异构体,主链有4个碳原子的正丁烷CH3CH2CH2CH3,主链有3个碳原子的异丁烷:CH3CH(CH3)2,
故答案为:CH3CH2CH2CH3;CH3CH(CH3)2;
(4)当该含氧有机物含有1个氧原子时,则剩余的式量是42,
| 42 |
| 14 |
故答案为:CH2=CH-CH2OH( 或CH3COCH3).
点评:本题考查有机物的分子式的确定,同分异构体的书写,题目难度不大,注意掌握碳原子数目≤5的同分异构体的书写方法.

练习册系列答案
相关题目
在一定条件下NO2与SO2气体发生反应,NO2(g)+SO2(g)?SO3(g)+NO(g)△H=-41.8kJ?mol-1.将NO2与SO2以体积比1:2置于密闭容器中发生上述反应,下列能说明反应达到平衡状态的是( )
| A、混合气体颜色保持不变 |
| B、体系压强保持不变 |
| C、SO3和NO的体积比保持不变 |
| D、每消耗1 mol SO3的同时生成1 mol NO2 |
下列关于摩尔质量的说法正确的是( )
| A、氯气的摩尔质量是71克 |
| B、HCl的摩尔质量为36.5 g/mol |
| C、1摩氢气的质量为2 g/mol |
| D、O2的摩尔质量为16g/mol |
 气态有机物 A在标准状况下密度为1.25g/L,A在一定条件下可以合成聚合物B,B可作食品包装袋.
气态有机物 A在标准状况下密度为1.25g/L,A在一定条件下可以合成聚合物B,B可作食品包装袋. (1)铝热反应原理
(1)铝热反应原理
 与
与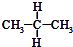
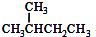 与
与