题目内容
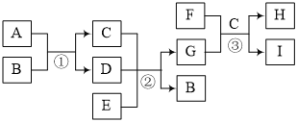
【题目】有关物质的转化关系如下图所示。A是红棕色固体,B是常见的强酸,C是常见的无色液体。E、F均为无色有刺激性气味的气体,其中E能使品红溶液褪色。G可用作补血剂,I是一种白色固体,在空气中最终变成红褐色。请回答下列问题:


(1)F的电子式为_____。
(2)写出反应②的离子方程式,并用单线桥标出电子转移的方向和数目_____。
(3)可确定反应②中金属离子已完全反应的试剂为_____(填化学式)。反应③的装置如上图所示,倒置漏斗的作用是_____。
(4)写出反应③的离子方程式:_____。
【答案】![]()
![]() KSCN 防止发生倒吸 2NH3+2H2O+Fe2+=Fe(OH)2↓+2NH4+(或2NH3·H2O+Fe2+=Fe(OH)2↓+2 NH4+)
KSCN 防止发生倒吸 2NH3+2H2O+Fe2+=Fe(OH)2↓+2NH4+(或2NH3·H2O+Fe2+=Fe(OH)2↓+2 NH4+)
【解析】
有关物质的转化关系如下图所示。
A是红棕色固体,则为氧化铁;
E能使品红溶液褪色,E为无色有刺激性气味的气体,则为二氧化硫;
B是常见的强酸,在根据E和D、C反应,生成B,说明B为硫酸,C为水;
F均为无色有刺激性气味的气体,I是一种白色固体,在空气中最终变成红褐色,说明F为氨气;
G可用作补血剂,说明是硫酸亚铁;
⑴F为氨气,其电子式为![]() ,故答案为
,故答案为![]() ;
;
⑵反应②是铁离子和二氧化硫发生氧化还原反应,其离子方程式为:SO2+2H2O+2Fe2+= 4H++2Fe2++SO42-,用单线桥标出电子转移的方向和数目![]() ,故答案为
,故答案为![]() ;
;
⑶可确定反应②中金属离子已完全反应即无铁离子,可用KSCN来确认,反应③的装置如上图所示,由于氨气极易溶于水,用倒置漏斗的作用是防倒吸,故答案为KSCN;防倒吸;
⑷反应③主要是亚铁离子和氨气、水发生反应,其离子方程式:2NH3+2H2O+Fe2+=Fe(OH)2↓+2NH4+(或2NH3·H2O+Fe2+=Fe(OH)2↓+2 NH4+)故答案为2NH3+2H2O+Fe2+=Fe(OH)2↓+2NH4+(或2NH3·H2O+Fe2+=Fe(OH)2↓+2 NH4+)。

【题目】硫及其化合物是重要的化工原料,某学习小组对某些硫的化合物性质和制备进行如下实验探究:
Ⅰ.探究实验一:将一定量的浓H2SO4与足量Zn置于装置A中充分反应,对反应后的气体X进行气体成分分析(水蒸气除外)。

回答下列问题:
(1)气体X中除水蒸气之外,还可能有的气体是______________________。
(2)B中的试剂可能是__________,酸性KMnO4溶液的作用是_____________。
(3)D、E装置用于证明气体X中的另一种组分,按照D、E装置顺序观察到的实验现象分别是___________、___________。
Ⅱ.探究实验二:制取硫代硫酸钠(Na2S2O3)并探究其性质。
(1)制取Na2S2O3(装置如下图,夹持装置省略)。

①装置B中生成Na2S2O3的同时也生成CO2,反应的离子方程式为___________。
②除搅拌和使用多孔球泡外,再写出一种可以提高B中吸收SO2效率的方法___________。
(2)探究Na2S2O3的性质(反应均在溶液中进行),请填空:
Na2S2O3性质 | 实验操作 | 实验现象 | |
探究1 | Na2S2O3溶液的酸碱性 | ____ | pH=8 |
探究2 | Na2S2O3的还原性 | 向新制的溴水中滴加Na2S2O3溶液 | __________ |






