题目内容
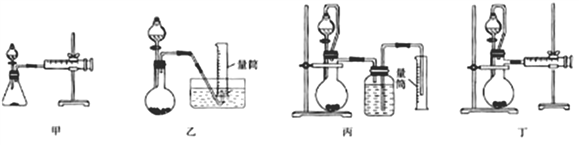
【题目】为了探究原电池和电解池的工作原理,某研究性学习小组分别用下图所示的装置进行实验。据图回答问题。

I.用图甲所示装置进行第一组实验时:
(1)在保证电极反应不变的情况下,不能替代Cu作电极的是_____ (填字母)。
A石墨 B. 镁 C.银 D.铂
(2)实验过程中,SO42-____(填“从左向右”“从右向左”或“不”)移动;滤纸上能观察到的现象是________________。
II.该小组同学用图乙所示装置进行第二组实验时发现,两极均有气体产生,且Y极处溶液逐渐变成紫红色;停止实验观察到铁电极明显变细,电解液仍然澄清。查阅资料知,高铁酸根(FeO42-)在溶液中呈紫红色。请根据实验现象及所查信息,回答下列问题:
(3)电解过程中,X极处溶液的OH-浓度____(填“增大”“减小”或“不变)。
(4)电解过程中,Y极发生的电极反应为___________________,_________________。
(5)电解进行一段时间后,若在X极收集到672mL气体,Y电板(铁电极)质量减小0.28g,则在Y极收集到气体为____mL(均己折算为标准状况时气体体积)。
(6)K2FeO4-Zn也可以组成碱性电池,K2FeO4在电池中作为正极材料,其电池反应总反应式为2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2,该电池正极发生的电极反应式为_______________。
【答案】B 从右向左 滤纸上有蓝色沉淀产生(答出“蓝色沉淀”或“蓝色斑点”即可) 增大 4OH--4e-=2H2O+O2↑ Fe-6e-+8OH-=FeO42-+4H2O 168 2FeO42-+6e-+5H2O=Fe2O3+10OH-
【解析】
I.甲装置是原电池,Zn作负极,Cu作正极,利用该原电池电解氢氧化钠溶液,结合原电池、电解池的工作原理解答。
II.乙装置是电解池,铁电极与电源正极相连,作阳极,铁失去电子,碳棒是阴极,氢离子放电,结合电极反应式以及电子得失守恒解答。
(1)甲装置是原电池,Zn作负极,Cu作正极。若要保证电极反应不变,则另一个电极的活动性只要比Zn弱即可。根据金属活动性顺序可知Mg>Zn,因此不能是Mg,答案选B。
(2)根据同种电荷相互排斥,异种电荷相互吸引的原则,实验过程中,SO42会向正电荷较多的Zn电极方向移动。即从右向左移动。利用该原电池电解氢氧化钠溶液,由于电极均是铜,在阳极上发生反应Cu-2e-=Cu2+,产生的Cu2+在溶液中发生反应Cu2++2OH-=Cu(OH)2↓,所以在滤纸上能观察到的现象是有蓝色沉淀产生。
(3)由图可知:X为阴极。电解过程中,X极上发生:2H++2e-=H2↑,破坏了水的电离平衡,水继续电离,最终导致溶液的c(OH-)增大,所以X极处溶液的c(OH-)增大。
(4)由于实验时发现,两极均有气体产生,且Y极处溶液逐渐变成紫红色;停止实验观察到铁电极明显变细,电解液仍然澄清。又因为高铁酸根(FeO42-)在溶液中呈紫红色,所以在电解过程中,Y极发生的电极反应为4OH-4e=2H2O+O2↑和Fe-6e+8OH=FeO42+4H2O;
(5)X电极产生氢气,n(H2)=0.672L÷22.4L/mol=0.03mol,n(e-)=0.06mol。在整个电路中电子转移数目相等,则4×n(O2)+6×(0.28g÷56g/mol)=0.06mol,解得n(O2)=0.0075mol,所以V(O2)=0.0075mol×22.4L/mol=0.168L=168mL;
(6)K2FeO4-Zn也可以组成碱性电池,Zn作负极,负极的电极反应式为3Zn-6e-+6OH-=3Zn(OH)2。K2FeO4在电池中作为正极材料,其电池反应为2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2。用总反应式减去负极电极式可得该电池正极发生的电极反应式为2FeO42+6e+5H2O=Fe2O3+10OH。

 黄冈冠军课课练系列答案
黄冈冠军课课练系列答案【题目】CO2既是温室气体,也是重要的化工原料,以CO2为原料可合成多种有机物。
(1)CO2可用于生产甲醇,已知:2CO2(g)+6H2(g) ![]() CH2=CH2(g)+4H2O(g) ΔH=QkJ/mol。一定条件下,按不同的投料比X(X=n(H2)/n(CO2))向某容积可变的恒压密闭容器中充入CO2、H2,测得不同投料比时CO2的转化率与温度的关系如图所示。
CH2=CH2(g)+4H2O(g) ΔH=QkJ/mol。一定条件下,按不同的投料比X(X=n(H2)/n(CO2))向某容积可变的恒压密闭容器中充入CO2、H2,测得不同投料比时CO2的转化率与温度的关系如图所示。

①X1_______X2(填“>”或“<”,后同),Q_______0。
②图中A、B、C三点对应的平衡常数KA、KB、KC的大小关系为______。
③TK时,在该容积可变的恒压密闭容器中发生上述反应,测得有关数据如下表所示:
物质的量(mol) 时间(min) | 0 | 5 | 10 | 15 | 20 |
H2(g) | 6.00 | 5.40 | 5.10 | 5.80 | 5.80 |
CO2(g) | 2.00 | 1.80 | 1.70 | 1.60 | 1.60 |
CH2=CH2(g) | 0 | 0.10 | 0.15 | 0.20 | 0.20 |
已知在10min时只改变了一个反应条件,用改变的条件可能是______。
④下列情况下能表明该反应达到平衡状态的是_____。
a.气体密度不变 b.混合气休的平均摩尔质量不变 c.消耗速率:2v(H2O)=v(CO2)
(3)常温下,用NaOH溶液作CO2捕捉剂不仅可以降低碳排放,而且可得到重要的化工产品Na2CO3。
① 若某次捕捉后得到pH=10的溶液,则溶液中c(CO32-):c(HCO3-)=______ [常温下K1(H2CO3)=4.4×10-7、K2(H2CO3)=5×10-11]。
② 欲用5L Na2CO3溶液将23.3 g BaSO4固体全都转化为BaCO3,则所用的Na2CO3溶液的物质的量浓度至少为_________。[已知:常温下Ksp(BaSO4)=1×10-7、Ksp(BaCO3)=2.5×10-6]。(忽略溶液体积积的变化)
【题目】为除去某物质中所含的杂质,周佳敏同学做了以下四组实验,其中她所选用的试剂或操作方法正确的是( )
序号 | 物质 | 杂质 | 除杂试剂或操作方法 |
① | NaCl溶液 | Na2CO3 | 加入盐酸,蒸发 |
② | FeSO4溶液 | CuSO4 | 加入过量铁粉并过滤 |
③ | H2 | CO2 | 依次通过盛有NaOH溶液和浓硫酸的洗气瓶 |
④ | NaNO3 | CaCO3 | 加稀盐酸溶解、过滤、蒸发、结晶 |
A.①②③
B.②③④
C.①③④
D.①②③④