题目内容
7.实验室欲配制100mL 2mol/L的KCl溶液,就配制该溶液的过程,请回答:(1)不需要的仪器是CF.
A.烧杯 B.100mL容量瓶 C.量筒 D.胶头滴管 E.玻璃棒 F.50mL容量瓶
(2)配制时用托盘天平,应称取KCl14.9g.
(3)配制该溶液时,一般可以分为以下几个步骤:
①称量 ②计算 ③溶解 ④摇匀 ⑤转移 ⑥洗涤 ⑦定容 ⑧装瓶贴签其正确的操作顺序为②①③⑤⑥⑦④⑧
(4)若容量瓶未干燥即用来配制溶液,实验结果将无影响,若定容时俯视刻度线,实验结果将偏高.(填“偏低”“偏高”“无影响”)
分析 (1)依据配制溶液的一般步骤选择需要的仪器;
(2)依据m=CVM计算需要溶质的质量;
(3)用固体配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶等,据此排序;
(4)分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析.
解答 解:(1)用固体配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀等,用到的仪器:托盘天平、药匙、玻璃棒、烧杯、容量瓶、胶头滴管,配制100mL 2mol/L的KCl溶液应选择100mL容量瓶,不需要的仪器:量筒、50mL容量瓶;
故答案为:CF;
(2)配制100mL 2mol/L的KCl溶液,需要溶质的质量m=2mol/L×0.1L×74.5g/mol=14.9g;
故答案为:14.9;
(3)用固体配制一定物质的量浓度溶液一般步骤:计算、称量、溶解、冷却、移液、洗涤、定容、摇匀、装瓶等,所以正确的操作顺序为:②①③⑤⑥⑦④⑧;
故答案为:②①③⑤⑥⑦④⑧;
(4)若容量瓶未干燥即用来配制溶液,对溶质的物质的量和溶液体积都不产生影响,溶液浓度无影响;
若定容时俯视刻度线,导致溶液体积偏小,溶液浓度偏高;
故答案为:无影响;偏高.
点评 本题考查了一定物质的量浓度溶液的配制,明确配制原理及操作步骤是解题关键,注意分析操作对溶质的物质的量和溶液体积的影响,依据C=$\frac{n}{V}$进行误差分析的方法,题目难度不大.

练习册系列答案
 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案
相关题目
2.对于反应X(g)+Y(g)?3Z(g)(正反应为吸热反应),下列可作为平衡状态的标志的是( )
①单位时间内,A、B生成C的分子数与分解C的分子数相等
②体系的温度不再变化
③外界条件不变时,A、B的浓度不随时间而变化
④体系的压强不再变化
⑤体系的分子总数不再变化.
①单位时间内,A、B生成C的分子数与分解C的分子数相等
②体系的温度不再变化
③外界条件不变时,A、B的浓度不随时间而变化
④体系的压强不再变化
⑤体系的分子总数不再变化.
| A. | ①③⑤ | B. | ②③④ | C. | ①③④⑤ | D. | ①②③④⑤ |
12.在一定条件下,向密闭容器中充入30mLCO和20mL水蒸气,使其反应,当反应CO(g)+H2O(g)?CO2(g)+H2(g)达到平衡时,水蒸气的体积分数与H2的体积分数相等,下列叙述错误的是( )
| A. | 平衡后CO的体积分数为40% | |
| B. | 平衡后CO的转化率为25% | |
| C. | 平衡后水的转化率为50% | |
| D. | 平衡后混合气体的平均相对分子质量为24 |
19.下列各组无色溶液的离子组在pH=l时能大量共存的是( )
| A. | NH4+、C1-、Mg2+、SO42- | B. | A13+、Cu2+、SO42-、C1- | ||
| C. | Ba2+、K+、NO3-、OH- | D. | Ca2+、Na+、C1-、A1O2- |
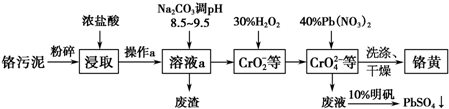
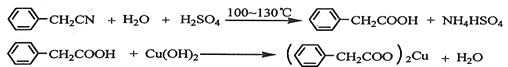
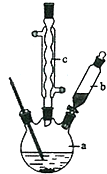 苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线:
苯乙酸铜是合成优良催化剂、传感材料--纳米氧化铜的重要前驱体之一.下面是它的一种实验室合成路线: