题目内容
16.罂粟碱是一种异喹啉型生物碱,其盐酸盐可用于治疗脑血栓、肢端动脉痉挛等.罂粟碱的合成方法如图: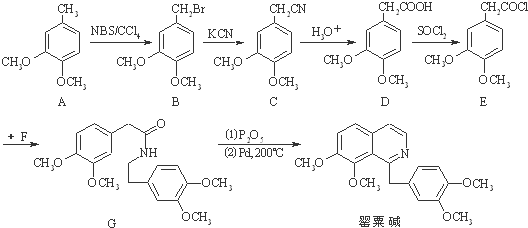
(1)G分子中的含氧官能团有肽键和醚键(填名称).
(2)B→C的转化属于取代反应(填反应类型).
(3)写出D→E的化学反应方程式
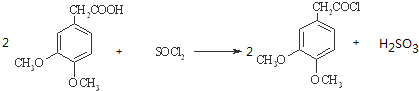 .
.(4)E和F发生取代反应生成G的同时有HCl生成,则F的结构简式是
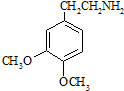 .
.(5)E的同分异构体有多种,写出一种符合下列要求的异构体X的结构简式:
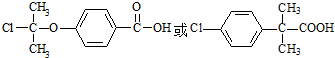 .
.Ⅰ.含氧官能团种类与D相同;
Ⅱ.核磁共振氢谱图中有4个吸收峰;
Ⅲ.属于芳香族化合物,苯环上一取代物有两种.
分析 (1)根据G的结构简式可知G中含氧官能团名称;
(2)比较B和C的结构简式可知,B中的溴原子被-CN取代;
(3)比较D和E的结构简式可知,D中的-OH被氯原子取代生成E;
(4)比较E和G的结构简式,利用元素守恒可写出F的结构简式;
(5)根据E的结构,结合Ⅰ.含氧官能团种类与D相同,即含醚键和羧基,Ⅱ.核磁共振氢谱图中有4个吸收峰,即分子中有4种等效氢,Ⅲ.属于芳香族化合物,苯环上一取代物有两种,即苯环上有两种等效氢,可写出X的结构简式;
解答 解:(1)根据G的结构简式可知G中含氧官能团名称为肽键、醚键,
故答案为:肽键、醚键;
(2)比较B和C的结构简式可知,B中的溴原子被-CN取代,B→C的转化属于取代反应,
故答案为:取代;
(3)比较D和E的结构简式可知,D中的-OH被氯原子取代生成E,反应方程式为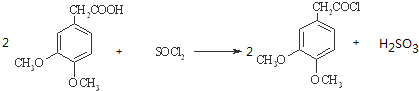 ,
,
故答案为: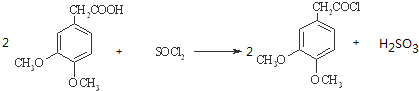 ;
;
(4)比较E和G的结构简式,利用元素守恒可知F的结构简式为 ,
,
故答案为: ;
;
(5)根据E的结构,结合条件Ⅰ.含氧官能团种类与D相同,即含醚键和羧基,Ⅱ.核磁共振氢谱图中有4个吸收峰,即分子中有4种等效氢,Ⅲ.属于芳香族化合物,苯环上一取代物有两种,即苯环上有两种等效氢,所以符合条件的X的结构简式为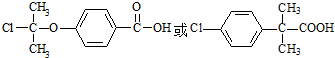 ,
,
故答案为: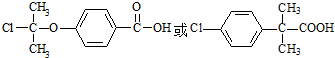 ;
;
点评 本题考查有机物的结构和性质,答题时注意有机官能团的性质及转化,侧重对基础知识的综合考查,难度中等.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案
相关题目
6.已知Fe3O4可表示成(FeO•Fe2O3),水热法制备Fe3O4纳米颗粒的总反应为:3Fe2++2S2O32-+O2+4OH-═Fe3O4+S4O62-+2H2O,下列说法正确的是( )
| A. | O2是氧化剂,Fe2+和S2O32-是还原剂 | |
| B. | 每生成1molFe3O4,则转移电子数为2mol | |
| C. | 参加反应的氧化剂与还原剂的物质的量之比为1:1 | |
| D. | 若有2molFe2+被氧化,则被Fe2+还原的O2为0.5mol |
4.下列说法正确的是( )
| A. | 固体NaCl不导电,所以NaCl是非电解质 | |
| B. | 蔗糖、酒精在水溶液和熔融状态时均不导电,所以它们是非电解质 | |
| C. | 铜、石墨均导电,所以它们是电解质 | |
| D. | CO2的水溶液能导电,所以CO2是电解质 |
11.下列各组热化学方程式的前者△H大于后者的是( )
①S(s)+O2(g)═SO2(g)△H1 S(g)+O2(g)═SO2(g)△H2
②2H2(g)+O2(g)═2H2O(g)△H3 2H2(g)+O2(g)═2H2O(l)△H4
③CaCO3(s)═CaO(s)+CO2(g)△H5 CaO(s)+H2O(l)═Ca(OH)2(s)△H6.
①S(s)+O2(g)═SO2(g)△H1 S(g)+O2(g)═SO2(g)△H2
②2H2(g)+O2(g)═2H2O(g)△H3 2H2(g)+O2(g)═2H2O(l)△H4
③CaCO3(s)═CaO(s)+CO2(g)△H5 CaO(s)+H2O(l)═Ca(OH)2(s)△H6.
| A. | 只有①③ | B. | 只有①② | C. | 只有②③ | D. | ①②③ |
1.钼(Mo)是一种过渡金属元素,通常用作合金及不锈钢的添加剂,这种元素可增强合金的强度、硬度、可焊性及韧性,还可增强其耐高温及耐腐蚀性能.如图是化工生产中制备金属钼的主要流程图,已知钼酸难溶于水.
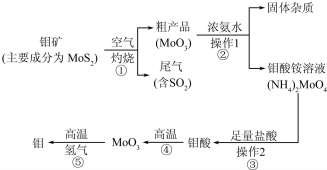
(1)写出反应①的化学方程式:2MoS2+7O2$\frac{\underline{\;高温\;}}{\;}$2MoO3+4SO2 .
(2)写出反应②的化学方程式:MoO3+2NH3•H2O=(NH4)2MoO4.
(3)反应①的尾气可以用碳酸钠溶液吸收.已知
根据表中提供的数据可知,在溶液中不能大量共存的微粒是
A.HCO3-、HSO3- B HCO3-、SO32-
C.HCO3-、H2SO3 D HSO3-、CO32-
向过量碳酸钠溶液中通人少量二氧化硫,写出反应的离子方程式:2CO32-+SO2+H2O=SO32-+2HCO3-.
(4)如果在实验室模拟操作1和操作2,则需要使用的主要玻璃仪器有烧杯、漏斗、玻璃棒.
(5)工业上制备还原性气体CO和H2的反应原理为CO2+CH4$\frac{\underline{\;高温\;}}{\;}$2CO+2H2,CH4+H2O$\frac{\underline{\;高温\;}}{\;}$CO+3H2.含甲烷体积分数为80%的10L(标准状况)天然气与足量二氧化碳和水蒸气的混合物在高温下反应,甲烷转化率为90%,用产生的还原性气体(CO和H2)还原MoO3制钼,理论上能生产钼的质量为41.1g(小数点后保留1位,钼的相对原子质量为96).

(1)写出反应①的化学方程式:2MoS2+7O2$\frac{\underline{\;高温\;}}{\;}$2MoO3+4SO2 .
(2)写出反应②的化学方程式:MoO3+2NH3•H2O=(NH4)2MoO4.
(3)反应①的尾气可以用碳酸钠溶液吸收.已知
| 化学式 | 电离常数 |
| H2SO3 | K1=1.3×10-2,K2=6.2×10-8 |
| H2CO3 | K1=4.3×10-7,K2=5.6×10-11 |
A.HCO3-、HSO3- B HCO3-、SO32-
C.HCO3-、H2SO3 D HSO3-、CO32-
向过量碳酸钠溶液中通人少量二氧化硫,写出反应的离子方程式:2CO32-+SO2+H2O=SO32-+2HCO3-.
(4)如果在实验室模拟操作1和操作2,则需要使用的主要玻璃仪器有烧杯、漏斗、玻璃棒.
(5)工业上制备还原性气体CO和H2的反应原理为CO2+CH4$\frac{\underline{\;高温\;}}{\;}$2CO+2H2,CH4+H2O$\frac{\underline{\;高温\;}}{\;}$CO+3H2.含甲烷体积分数为80%的10L(标准状况)天然气与足量二氧化碳和水蒸气的混合物在高温下反应,甲烷转化率为90%,用产生的还原性气体(CO和H2)还原MoO3制钼,理论上能生产钼的质量为41.1g(小数点后保留1位,钼的相对原子质量为96).
8.常温下,下列溶液中各微粒浓度关系或pH判定不正确的是( )
| A. | 将5 mL 0.02 mol/L的H2SO4溶液与5 mL 0.02 mol/L NaOH溶液充分混合,若混合后溶液的体积为10 mL,则混合液的pH=2 | |
| B. | 某物质的溶液中由水电离的c(H+)=1×10-amol/L,若a>7,则pH一定为14-a | |
| C. | pH相等的①CH3COONa ②C6H5ONa ③NaHCO3溶液中,c(Na+)大小关系:①>③>② | |
| D. | CH3COONa溶液中加入少量KNO3固体后的碱性溶液一定有:c(Na+)+c(H+)=c(CH3COO-)+c(OH-) |
6.下列变化中必须加入适当的氧化剂才能实现的是( )
| A. | MnO2→Mn2+ | B. | PCl3→PCl5 | C. | HCl→H2 | D. | SO2→SO32- |
