题目内容
一定温度下,10 mL 0.4 mol/LH2O2溶液发生催化分解。不同时刻测得生成O2的体积(已折算为标准状况)如下表:
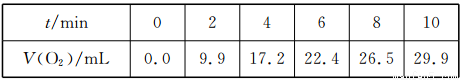
下列叙述错误的是(溶液体积变化忽略不计)( )
A.反应至6 min时,c(H2O2)=0.20mol/L
B.反应至6 min时,H2O2分解了40%
C.0~6 min的平均反应速率:v(H2O2)≈3.3×10-2 mol.L-1.min-l
D.6~10 min的平均反应速率:可(H2O2) <3.3×10-2 mol.L-1.min-l
练习册系列答案
相关题目


 CaO(s)+CO2(g)达到平衡,下列说法正确的是
CaO(s)+CO2(g)达到平衡,下列说法正确的是 Na2CO3(s)+10H2O(1),热效应为△H3。则下列判断正确的是( )
Na2CO3(s)+10H2O(1),热效应为△H3。则下列判断正确的是( ) 4Fe(OH)3+8OH-+3O2。图1是25℃时K2FeO4在不同pH溶液中浓度的变化情况,图2是K2FeO4在不同温度时溶液浓度的变化情况。
4Fe(OH)3+8OH-+3O2。图1是25℃时K2FeO4在不同pH溶液中浓度的变化情况,图2是K2FeO4在不同温度时溶液浓度的变化情况。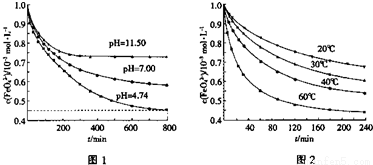

 HCl + HClO,实验测得约有三分之一的氯气与水发生了反应。反应Cl2+H2O
HCl + HClO,实验测得约有三分之一的氯气与水发生了反应。反应Cl2+H2O P4(s,白磷)+
P4(s,白磷)+ O2(g)===
O2(g)===