题目内容
在日常生活中为什么常用热的纯碱溶液洗涤沾有油脂的器皿?
考点:盐类水解的应用,油脂的性质、组成与结构
专题:盐类的水解专题,有机化学基础
分析:油脂能够与碱性溶液反应生成易溶于水的物质,故可用碱性溶液除去器皿上的油污;纯碱为碳酸钠,溶液中碳酸根离子部分水解使溶液显示碱性,碱性溶液能够与油脂发生反应,且碳酸根离子的水解为吸热反应,热的纯碱溶液中碱性更强,除去油污的效果更好.
解答:
解:器皿上的油污属于油脂,能够与碱性溶液反应生成可溶性物质,从而达到除去油污的目的;
纯碱为碳酸钠,碳酸钠为盐,溶液中电离出钠离子和碳酸根离子,碳酸根离子水解分步进行:CO32-+H2O?HCO3-+OH-、HCO3-+H2O?H2CO3+OH-,碳酸根离子的水解为吸热反应,升高温度可以促进碳酸根离子的水解,溶液中氢氧根离子浓度增大,碱性增强,更有利于除去器皿上沾有的油脂,
答:纯碱溶液呈碱性,热的纯碱溶液中碱性增强,能够更好的与油脂反应生成可溶于水的物质而洗去油污.
纯碱为碳酸钠,碳酸钠为盐,溶液中电离出钠离子和碳酸根离子,碳酸根离子水解分步进行:CO32-+H2O?HCO3-+OH-、HCO3-+H2O?H2CO3+OH-,碳酸根离子的水解为吸热反应,升高温度可以促进碳酸根离子的水解,溶液中氢氧根离子浓度增大,碱性增强,更有利于除去器皿上沾有的油脂,
答:纯碱溶液呈碱性,热的纯碱溶液中碱性增强,能够更好的与油脂反应生成可溶于水的物质而洗去油污.
点评:本题考查了盐的水解原理及其应用,题目难度不大,试题侧重基础知识的考查,注意掌握油脂的组成、性质,明确盐的水解原理及其应用,试题培养了学生灵活应用所学知识的能力.

练习册系列答案
 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案
相关题目
已知:CH4(g)+2O2(g)→CO2(g)+2H2O(l)△H═-Q1 kJ?mol-1
H2(g)+
O2(g)═H2O(g)△H=-
Q2 kJ?mol-1
H2(g)+
O2(g)═H2O(l)△H3=-
Q3kJ?mol-1
常温下取体积比为4:1的甲烷和氢气的混合气体11.2L(标准状况),经完全燃烧后恢复到室温,则放出的热量为( )
H2(g)+
| 1 |
| 2 |
| 1 |
| 2 |
H2(g)+
| 1 |
| 2 |
| 1 |
| 2 |
常温下取体积比为4:1的甲烷和氢气的混合气体11.2L(标准状况),经完全燃烧后恢复到室温,则放出的热量为( )
| A、0.4 Q1+0.05 Q3 |
| B、0.4 Q2+0.05 Q3 |
| C、0.4 Q1+0.1 Q3 |
| D、0.4 Q1+0.2 Q2 |
下列不是水玻璃用途的是( )
| A、肥皂填料 |
| B、木材防火剂 |
| C、纸板黏胶剂 |
| D、建筑装饰材料 |

 (4)△H3=
(4)△H3=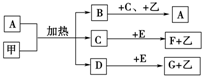 已知化合物A、B、C、D、E、F、G和单质甲、乙所含元素均为短周期元素,A的浓溶液与甲能发生如图所示的反应,甲是常见的固体单质,乙是常见的气体单质,B是无色气体,是主要的大气污染物之一,请根据图示回答问题.
已知化合物A、B、C、D、E、F、G和单质甲、乙所含元素均为短周期元素,A的浓溶液与甲能发生如图所示的反应,甲是常见的固体单质,乙是常见的气体单质,B是无色气体,是主要的大气污染物之一,请根据图示回答问题.
