题目内容
重铬酸钾是一种常见的强氧化剂。实验室以精选铬铁矿(主要成分可表示为FeO.Cr2O3,还含有SiO2、Al2O3等杂质)为原料制备重铬酸钾晶体(K2Cr2O7,式量294)的流程如下:
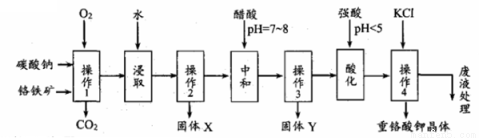
请回答下列问题:
⑴操作1中发生的反应有:
4FeO·Cr2O3 + 8Na2CO3 + 7O2 = 8Na2CrO4 + 2Fe2O3 + 8CO2↑
Na2CO3 + Al2O3 = 2NaAlO2 + CO2↑
Na2CO3 + SiO2 = Na2SiO3 + CO2↑
该步骤在常温下的反应速率较慢,为使反应速率增大,可采取的措施是 (写出两条)
⑵固体Y中主要含有 。(填写化学式)
⑶酸化步骤使含铬物质发生了转化为_________,请写出离子反应方程式 。
⑷操作4中的化学反应在溶液中能发生的可能理由是 ,获得晶体的操作依次是:加入KCl固体,在水浴上加热浓缩至 ,冷却结晶,抽滤、洗涤、干燥。
⑸通过下列实验可测定产品中重铬酸钾的质量分数:
称取重铬酸钾试样1.470g,用100mL容量瓶配制成溶液。移取25.00mL溶液于碘量瓶中,加入适量稀硫酸和足量碘化钾(铬的还原产物为Cr3+),放于暗处5min。然后加入一定量的水,加入淀粉指示剂,用0.1500mol/L Na2S2O3标准溶液滴定,共消耗标准液36.00mL。滴定时发生的反应的离子方程式为:
I2 + 2S2O32- = 2I- + S4O62-
则所测定产品中重铬酸钾的纯度为 。
⑹有关上述实验过程中涉及的部分实验操作的描述,正确的是 。
A.粗产品若要进一步提纯,可以采用重结晶的方法
B.配制溶液时,用托盘天平称取试样后,一般经溶解、转移(含洗涤)、定容等步骤,配制成100mL溶液
C.滴定时,当最后一滴标准溶液滴入时,溶液变为蓝色,且半分钟内不变色,可判断滴定终点
D.滴定终点时俯视读数,测定结果偏低
 名校课堂系列答案
名校课堂系列答案根据表中信息判断,下列选项不正确的是( )
序号 | 反应物 | 产物 |
① | KMnO4 、H2O2、H2SO4 | K2SO4、MnSO4 … |
② | Cl2、FeBr2 | FeC13、FeBr3 |
③ | MnO4- | Cl2、Mn2+ … |
A.第①组反应的其余产物为H2O和O2
B.第②组反应中Cl2与FeBr2的物质的量之比为1:2
C.第③组反应中生成1 mol C12,转移电子2 mol
D.氧化性由强到弱顺序为MnO4->C12>Fe3+>Br2
通过观察化学实验现象,分析归纳出正确的结论,是学习化学科学最基本的技能之一。下列由实验现象得出正确结论的是( )
选项 | 实验现象 | 结 论 |
A | 把相同大小的一块铝和镁分别投入相同浓度的NaOH 溶液中:铝溶解有气泡放出,而镁没有任何变化 | 由此得出:铝的金属性比镁强 |
B | 取一块铝箔,用酒精灯点燃:铝箔只熔化成液体而没有脱落 | 由此得出:铝不易氧化 |
C | 向氯化铵溶液中投人一铝片:铝片上产生大量气泡 | 由此得出:该气体是氨气 |
D | 向氯化铝溶液中逐滴滴加NaOH溶液至过量:先产生白 色沉淀,后沉淀逐渐溶解,最后沉淀完全消失 | 由此得出:氢氧化铝能溶于强碱溶液 |



 Q>0),则下列分析正确的是
Q>0),则下列分析正确的是