题目内容
根据以下3个热化学方程式:
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H=-Q1kJ/mol
2H2S(g)+O2(g)=2S (s)+2H2O(l)△H=-Q2kJ/mol
2H2S(g)+O2(g)=2S (s)+2H2O(g)△H=-Q3kJ/mol
判断Q1、Q2、Q3三者关系正确的是( )
2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H=-Q1kJ/mol
2H2S(g)+O2(g)=2S (s)+2H2O(l)△H=-Q2kJ/mol
2H2S(g)+O2(g)=2S (s)+2H2O(g)△H=-Q3kJ/mol
判断Q1、Q2、Q3三者关系正确的是( )
| A、Q1>Q2>Q3 |
| B、Q1>Q3>Q2 |
| C、Q3>Q2>Q1 |
| D、Q2>Q1>Q |
考点:反应热的大小比较
专题:
分析:三个反应都为放热反应,物质发生化学反应时,生成液态水比生成气态水放出的热量多,反应越完全,放出的热量越多,以此解答该题.
解答:
解:已知①2H2S(g)+3O2(g)=2SO2(g)+2H2O(l)△H=-Q1 kJ/mol,
②2H2S(g)+O2(g)=2S (s)+2H2O(l)△H=-Q2 kJ/mol,
③2H2S(g)+O2(g)=2S (s)+2H2O(g)△H=-Q3kJ/mol,
①与②相比较,由于S→SO2放热,则Q1>Q2,
②与③相比较,由于H2O(l)→H2O(g)吸热,则Q2>Q3,
则Q1>Q2>Q3,
故选A.
②2H2S(g)+O2(g)=2S (s)+2H2O(l)△H=-Q2 kJ/mol,
③2H2S(g)+O2(g)=2S (s)+2H2O(g)△H=-Q3kJ/mol,
①与②相比较,由于S→SO2放热,则Q1>Q2,
②与③相比较,由于H2O(l)→H2O(g)吸热,则Q2>Q3,
则Q1>Q2>Q3,
故选A.
点评:本题考查反应热的大小比较,题目难度中等,本题注意从物质反应的程度以及物质的聚集状态的角度比较反应热的大小.

练习册系列答案
 轻松夺冠全能掌控卷系列答案
轻松夺冠全能掌控卷系列答案
相关题目
室温将等物质的量的NaCN和HCN溶于一定量水中,再加入适量稀盐酸,调整溶于pH=7.下列说法正确的是( )
| A、未加入稀盐酸之前:c(HCN)>c(Na+)>c(CN-)>c(OH-)>c(H+) |
| B、加稀盐酸后溶液中c(HCN)+c(CN-)=c(Na+) |
| C、PH=7时,溶液中:c(CN-)=c(Na+) |
| D、加稀盐酸后H2O的电离程度减小 |
在密闭容器中进行合成氨的反应:N2 (g)+3H2 (g)?2NH3(g)达到平衡后,当其它条件不变时,将平衡体系中各物质的浓度增加到原来的2倍,其结果是( )
| A、平衡向逆反应方向移动 |
| B、达新平衡时,c(N2)较原平衡变小 |
| C、达新平衡时,混合气体的密度变小 |
| D、达新平衡时正、逆反应速率均比原平衡变大 |
决定化学反应速率的主要因素是( )
| A、使用催化剂 |
| B、反应温度 |
| C、反应物本身的性质 |
| D、反应物的浓度 |
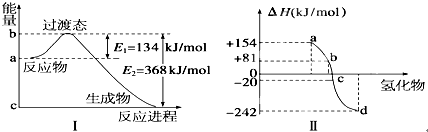
化学反应N2+3H2=2NH5的能量变化如图所示,该反应化学方程式是( )


| A、N2(g)+3H2(g)=2NH2(1);△H=2(a-b-c)KJ?mol-1 | ||||
| B、N2(g)+3H2(g)=2NH5(g);△H=2(b-a)KJ?mol-1 | ||||
C、
| ||||
D、
|
下列关于能量转换的认识中,不正确的是( )
| A、AgBr见光分解时,主要是光能转化为化学能 |
| B、甲烷燃烧是将全部的化学能转化为热能 |
| C、电池长时间使用会发热,说明部分化学能转变成热能 |
| D、光合作用是将太阳能转化成化学能 |
A和B是同周期相邻的元素,A和C是同主族相邻的元素,已知三种非金属元素A、B、C的原子序数依次增加,则下列说法正确的是( )
| A、原子半径A>B>C |
| B、元素的非金属性C>B>A |
| C、原子的得电子能力B>A>C |
| D、电子层数A=C>B |
下列反应的离子方程式正确的是( )
| A、乙酸乙酯与氢氧化钠溶液反应:CH3COOCH2CH3+OH--→CH3COO-+CH3CH2O-+H2O | ||
| B、醋酸溶液与新制氢氧化铜反应:2H++Cu(OH)2-→Cu2++2H2O | ||
C、苯酚钠溶液中通入少量二氧化碳:2 +CO2+H2O +CO2+H2O
 +CO32- +CO32- | ||
D、乙醛溶液与新制氢氧化铜悬浊液共热CH3CHO+2Cu(OH)2+OH_
|