题目内容
13.对于混合物的分离或提纯,常采用的方法有:过滤、蒸发、蒸馏、萃取、渗析、加热分解等.下列各组混和物的分离或提纯应采用什么方法?(1)除去氧化钙中的碳酸钙可用加热分解的方法.
(2)实验室中制取的Fe(OH)3胶体中常常含有杂质Cl-离子.可用渗析的方法除去Fe(OH)3胶体中混有的杂质Cl-离子.
(3)除去乙醇中溶解的微量食盐可采用蒸馏的方法.
(4)粗盐中含有不溶性的泥沙、可溶性的氯化钙、氯化镁及一些硫酸盐.对粗盐中的这些杂质可采用过滤和蒸发的方法除去(在操作过程中可以加入适当试剂).
分析 (1)碳酸钙加热分解生成CaO;
(2)离子可透过半透膜,而胶体不能透过;
(3)乙醇易挥发;
(4)不溶性的泥沙可过滤除去,而可溶性的氯化钙、氯化镁及一些硫酸盐加试剂转化为沉淀后除去,最后蒸发得到NaCl.
解答 解:(1)除去氧化钙中的碳酸钙可用加热分解的方法,故答案为:加热分解;
(2)可用渗析的方法除去Fe(OH)3胶体中混有的杂质Cl-离子,故答案为:渗析;
(3)除去乙醇中溶解的微量食盐可采用蒸馏的方法,故答案为:蒸馏;
(4)不溶性的泥沙可过滤除去,而可溶性的氯化钙、氯化镁及一些硫酸盐加试剂转化为沉淀后除去,最后蒸发得到NaCl,则采用过滤、蒸发可除杂,
故答案为:过滤;蒸发.
点评 本题考查混合物分离、提纯的方法及选择,为高频考点,把握物质的性质及性质差异、混合物分离方法为解答的关键,注重实验基础知识和基本技能的考查,注意有机物性质,题目难度不大.

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
9.下列各组离子,在溶液中可以大量共存的是( )
| A. | Na+、Ba2+、SO${\;}_{4}^{2-}$ | B. | K+、H+、OH- | ||
| C. | H+、CO${\;}_{3}^{2-}$、NO${\;}_{3}^{-}$ | D. | Na+、NO${\;}_{3}^{-}$、CO${\;}_{3}^{2-}$ |
8.“纳米材料”是粒子直径为1-100nm的材料,纳米碳就是其中一种,若将纳米碳均匀地分散到蒸馏水中所形成的物质,下列说法正确的是( )①是溶液②种置后会析出黑色沉淀③能产生丁达尔效应④能透过滤纸⑤不能透过滤纸⑥是胶体.
| A. | ①④⑤ | B. | ③④⑥ | C. | ②③⑤ | D. | ②③⑥ |
18.下列反应属于取代反应的是( )
| A. | 催化剂作用下,环氧丙烷和二氧化碳制备全降解塑料 | |
| B. | 催化剂作用下,乙烯和水制乙醇反应 | |
| C. | 乙醇在铜催化作用下与氧气的反应 | |
| D. | 甲烷和氯气光照条件下反应 |
2.下列有关化学用语使用正确的是( )
| A. | 硫原子的结构示意图: | |
| B. | ${\;}_{1}^{1}{H}_{2}$、${\;}_{1}^{2}$H2、${\;}_{1}^{3}{H}_{2}$是氢的三种同位素 | |
| C. | 原子核内有10个中子的氧原子${\;}_{8}^{18}O$ | |
| D. | 金刚石、石墨、甲烷属于同素异形体 |
3.如图所示的有机物可发生的反应类型有①取代 ②加成 ③消去 ④氧化( )

| A. | ①②③ | B. | ②③④ | C. | ①③④ | D. | ①②④ |
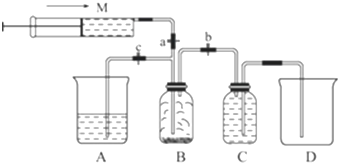
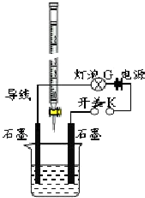 某温度下,水的离子积Kw=l×10-13.有酸溶液A,pH=a;碱溶液B,pH=b.为测定A、B混合后溶液导电性的变化以及探究A、B的相关性质,某同学设计了如图所示的实验装置.
某温度下,水的离子积Kw=l×10-13.有酸溶液A,pH=a;碱溶液B,pH=b.为测定A、B混合后溶液导电性的变化以及探究A、B的相关性质,某同学设计了如图所示的实验装置.