题目内容
4.用NA表示阿伏加德罗常数,下列叙述正确的是( )| A. | 标准状况下,22.4L H2O的分子数为 NA | |
| B. | 常温常压下,1mol甲基(-CH3)所含的电子数为10NA | |
| C. | 2.3g金属钠反应生成Na2O2时失去的电子数为0.1NA | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为NA |
分析 A、标况下水为液态;
B、甲基不显电性;
C、求出钠的物质的量,然后根据钠反应后变为+1价来分析;
D、溶液体积不明确.
解答 解:A、标况下水为液态,故不能根据气体摩尔体积来计算其物质的量和分子个数,故A错误;
B、甲基不显电性,故1mol甲基中含9NA个电子,故B错误;
C、2.3g钠的物质的量为0.1mol,而钠反应后变为+1价,故0.1mol钠失去0.1NA个电子,故C正确;
D、溶液体积不明确,故溶液中的氯离子的个数无法计算,故D错误.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案
相关题目
14.有如下两个反应①H2+Cl2$\frac{\underline{\;光照\;}}{\;}$2HCl ②2HCl$\frac{\underline{\;高温\;}}{\;}$H2+Cl2关于这两个反应的叙述中正确的是( )
| A. | ①②两个反应互为可逆反应 | B. | ①②两反应都是放热反应 | ||
| C. | ②反应是热能转变为化学能 | D. | ①反应是热能转变为化学能 |
15.下列反应属于消去反应的是( )
| A. | CH3CH2OH→CH2=CH2↑+H2O | B. | 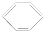 +Br2→ +Br2→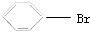 +HBr +HBr | ||
| C. | CH3CHO+H2→CH3CH2OH | D. | CH4+2O2→CO2+2H2O |
12.能用于鉴别甲烷和乙烯的试剂是( )
| A. | 水 | B. | 酸性高锰酸钾溶液 | ||
| C. | 苛性钠溶液 | D. | 四氯化碳溶液 |
19.小明是一个勤于动手、善于动脑,更善于创新的中学生,他看到家中购买的某品牌的“加碘食盐”包装袋上有部分文字说明:
(1)由食用方法、贮藏指南中,可以推测碘酸钾具有的化学性质之一是不稳定,遇光和热易分解.
(2)在查询了KIO3的性质后,KIO3有氧化性,可以发生IO3-+5I-+6H+═3I2+3H2O反应,他想在家中亲自检测一下该品牌的食盐是否真的含有碘,思考后他觉着还必须求助实验老师或到实验用品店购买KI试剂或淀粉KI试纸(一种实验用品)或将家中海带烧成灰烬后的水溶液来代替.
| 配料 | 氯化钠、碘酸钾 |
| 含碘量 | (40~50)mg/kg(以I计) |
| 保质期 | 18个月 |
| 食用方法 | 勿长时间炖炒 |
| 贮藏指南 | 避热、避光、密封、防潮 |
(2)在查询了KIO3的性质后,KIO3有氧化性,可以发生IO3-+5I-+6H+═3I2+3H2O反应,他想在家中亲自检测一下该品牌的食盐是否真的含有碘,思考后他觉着还必须求助实验老师或到实验用品店购买KI试剂或淀粉KI试纸(一种实验用品)或将家中海带烧成灰烬后的水溶液来代替.
9.下列各组离子在指定溶液中可能大量共存的是( )
| A. | 通入足量SO2的溶液中:Fe2+、Na+、SO42-、ClO- | |
| B. | 常温下,c(H+)═$\sqrt{{K}_{w}}$的溶液中:Na+、Fe3+、HCO3-、K+ | |
| C. | 水电离出的c(OH-)=10-13 mol/L的溶液中:Ba2+、Cl-、NO3-、I- | |
| D. | 遇酚酞显红色的溶液中:AlO2-、HCO3-、K+、NH4+ |
16.入夏以来,消防官兵扑灭了黑龙江、内蒙古三起特大森林火灾.开辟防火带(用于防火的通道)是灭火的重要措施之一,在树林中间开辟防火带的主要目的是( )
| A. | 便于消防人员快速通行 | B. | 将可燃物与火源隔离 | ||
| C. | 减少可燃物与空气的接触面积 | D. | 降低可燃物的着火点 |
13.一定量的甲烷在O2不足的情况下燃烧,得到CO、CO2和H2O的总质量是14.4g,若其中水的质量是7.2g,则CO的质量是( )
| A. | 2.8g | B. | 4.4g | ||
| C. | 5.6g | D. | 在2.8g和5.6g之间 |
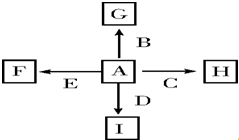 图中A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.
图中A、B、C、D、E是单质,G、H、I、F是B、C、D、E分别和A形成的二元化合物.