题目内容
【题目】用标准浓度氢氧化钠的溶液来滴定未知浓度的盐酸,下列操作中会使盐酸测定的浓度偏大的是( )
①碱式滴定管用蒸馏水洗净后未用标准溶液润洗
②锥形瓶中盛有少量蒸馏水,再加待测液
③酸式滴定用蒸馏水洗净后,未用盐酸润洗
④滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失
⑤滴定后观察碱式滴定管读数时,俯视刻度线
A.①④B.①③C.②③D.④⑤
【答案】A
【解析】
盐酸与氢氧化钠溶液进行反应,二者的物质的量相等,则c(HCl)=![]() ,在分析误差时,不管实际情况如何,都认为
,在分析误差时,不管实际情况如何,都认为![]() 是一个定值,盐酸的浓度只受NaOH体积变化的影响。
是一个定值,盐酸的浓度只受NaOH体积变化的影响。
①碱式滴定管用蒸馏水洗净后未用标准溶液润洗,V(NaOH)偏大,c(HCl)偏大;
②锥形瓶中盛有少量蒸馏水,再加待测液,V(NaOH)不变,c(HCl)不变;
③酸式滴定管用蒸馏水洗净后,未用盐酸润洗,V(NaOH)偏小,c(HCl)偏小;
④滴定前碱式滴定管尖端气泡未排除,滴定后气泡消失,V(NaOH)偏大,c(HCl)偏大;
⑤滴定后观察碱式滴定管读数时,俯视刻度线,V(NaOH)偏小,c(HCl)偏低。
综合以上分析,①④操作使盐酸测定的浓度偏大,符合题意。
故选A。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
【题目】用图所示装置检验乙烯时不需要除杂的是
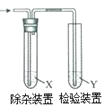
乙烯的制备 | 试剂X | 试剂Y | |
A | CH3CH2Br与NaOH乙醇溶液共热 | H2O | KMnO4酸性溶液 |
B | CH3CH2Br与NaOH乙醇溶液共热 | H2O | Br2的CCl4溶液 |
C | CH3CH2OH与浓H2SO4共热至170℃ | NaOH溶液 | KMnO4酸性溶液 |
D | CH3CH2OH与浓H2SO4共热至170℃ | NaOH溶液 | Br2的CCl4溶液 |