题目内容
下表为元素周期表的一部分。
|
族 周期 |
Ⅰ A |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
|
1 |
① |
|
|
|
|
|
|
|
2 |
|
|
|
⑥ |
|
⑦ |
⑧ |
|
3 |
② |
④ |
⑤ |
|
|
|
⑨ |
|
4 |
③ |
|
|
|
|
|
⑩ |
请参照元素①—⑩在表中的位置,用化学符号回答下列问题:
(1)元素⑩的电子排布式是______。
(2)在①—⑩中P轨道上有两个未成对电子的元素是______。
(3)在①—⑩中原子半径最大的是______。
(4)②、④、⑤、⑨离子的半径最小的是______。
(5)元素①和⑦的形成化合物和元素⑨的单质发生反应的离子方程式为______。
(6)元素②和⑤的最高价氧化物对应水化物相互反应的化学方程式为______。
(7)4.6g元素②的单质投入到足量的重水中,则产生的气体中含有______mol中子。
(8)等物质的量的元素⑧的单质和元素②的最高价氧化物对应水化物的恰好完全反应,生成三种产物,产物之一是由两种元素形成的气体化合物,则反应的化学方程式为____________,还原产物是______。
【答案】
(1)1S22S2263S23P63d104S24P5 (1分)
(2)C、O (1分)
(3)K (1分)
(4)Al3+ (1分)
(5)Cl2+H2O=H++Cl-+HClO (2分)
(6)NaOH+Al(OH)3=NaAlO2+2H2O (2分)
(7)0.2 (2分)
(8)2F2+2NaOH=2NaF+OF2↑+H2O (2分) NaF、OF2 (2分)

练习册系列答案
 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案
相关题目








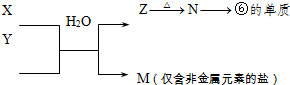
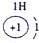
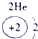
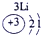
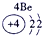
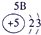
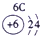
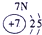
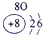
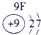
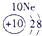
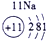





 表示的是
表示的是