题目内容
关于气体摩尔体积的理解正确的是( )
| A、气体摩尔体积的数值是固定不变的 |
| B、0℃,101kPa的条件下,气体的摩尔体积都约为22.4L |
| C、气体摩尔体积的数值与外界的温度和压强有关 |
| D、非标准状况下,气体的摩尔体积不可能是22.4L/mol |
考点:气体摩尔体积
专题:化学用语专题
分析:A.气体的摩尔体积由温度和压强决定;
B.摩尔体积的单位为L/mol;
C.气体的摩尔体积由温度和压强决定;
D.并不是只有在标准状况下Vm=22.4L/mol,Vm取决于温度和压强的大小.
B.摩尔体积的单位为L/mol;
C.气体的摩尔体积由温度和压强决定;
D.并不是只有在标准状况下Vm=22.4L/mol,Vm取决于温度和压强的大小.
解答:
解:A.气体的摩尔体积由温度和压强共同决定的,温度、压强改变,气体摩尔体积就变,故A错误;
B.摩尔体积的单位为L/mol,0℃,101kPa的条件下,气体的摩尔体积都约为22.4L/mol,故B错误;
C.气体的摩尔体积由温度和压强共同决定的,温度、压强改变,气体摩尔体积就变,故C正确;
D.根据PV=nRT可知,并不是只有在标准状况下Vm=22.4L/mol,Vm取决于温度和压强的大小,故D错误;
故选C.
B.摩尔体积的单位为L/mol,0℃,101kPa的条件下,气体的摩尔体积都约为22.4L/mol,故B错误;
C.气体的摩尔体积由温度和压强共同决定的,温度、压强改变,气体摩尔体积就变,故C正确;
D.根据PV=nRT可知,并不是只有在标准状况下Vm=22.4L/mol,Vm取决于温度和压强的大小,故D错误;
故选C.
点评:本题考查气体摩尔体积的概念,题目难度不大,注意在标准状况下,Vm=22.4L/mol,其它条件下也有可能为22.4L/moL.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列变化中,一定不存在化学能与热能相互转化的是( )
| A、酸碱中和反应 | B、白磷自燃 |
| C、燃放爆竹 | D、干冰气化 |
下列说法不正确的是( )
| A、磷酸的摩尔质量与6.02×1023个磷酸分子的质量在数值上相等 |
| B、6.02×1023个氮分子和6.02×1023个氢分子的质量比等于14:1 |
| C、32g氧气所含的原子数目为2×6.02×1023 |
| D、CO的摩尔质量与NA个CO分子质量相同 |
NA表示阿伏加德罗常数的值,下列说法正确的是 ( )
| A、常温常压下3.2 g O2中含有的氧原子数目为0.2 NA |
| B、101 kPa 0℃时,22.4 L氢气中含有NA个氢原子 |
| C、标准状况下,2.24 L 四氯化碳含有的碳原子数目为0.1NA |
| D、标准状况下,22.4LCl2和HCl的混合气体所含分子总数为2NA |
下列说法中正确的是(NA代表阿伏伽德罗常数)( )
| A、28g N2和28g CO所含的分子数都是NA |
| B、32g O3和32g O2所含的分子数都是NA |
| C、28g CO和44g CO2所含的氧原子数都是2NA |
| D、98g H2SO4和98g H3PO4所含的氧原子数都是4NA |
下列反应的离子方程式正确的是( )
| A、NaHSO4溶液和Ba(OH)2溶液反应后呈中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O |
| B、实验室制取CO2:CO32-+2H+═CO2↑+H2O |
| C、铁和硝酸银溶液反应:Fe+Ag+=Ag+Fe3+ |
| D、硫酸铜溶液跟氢氧化钡溶液反应:Ba2++2OH-+Cu2++SO42-=BaSO4↓+Cu(OH)2↓ |
0.5mol O2中含有( )
| A、1个氧原子 |
| B、6.02×1023个氧分子 |
| C、1mol氧原子 |
| D、0.5个氧分子 |
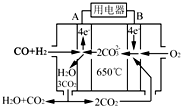 研究NO2、SO2、CO等大气污染气体的测量及处理具有重要意义.
研究NO2、SO2、CO等大气污染气体的测量及处理具有重要意义.