题目内容
5.已知在酸性溶液中,下列物质氧化 KI 时,自身发生如下变化:ClO3-→Cl-;MnO4-→Mn2+;Cl2→2Cl-;IO3-→I2.如果分别用这些物质氧化的 KI生成等量的 I2,消耗他们物质的量最少的是( )| A. | ClO3- | B. | MnO4- | C. | Cl2 | D. | IO3- |
分析 在四个反应中氧化剂不一样,而还原剂均为碘化钾中的碘离子,如果分别用这些物质氧化的 KI生成等量的 I2,如氧化物不含碘元素,则化合价变化最大的物质的量最少,如含碘元素,则含碘氧化剂的物质的量最少,以此来解答.
解答 解:氧化I-时,ClO3-→Cl-得到6个电子,MnO4-→Mn2+得到5个电子,Cl2→2Cl-得到2个电子,IO3-→I2得到5个电子,
但IO3-由于也被还原为I2,则消耗他们物质的量最少的是IO3-,
故选D.
点评 本题考查氧化还原反应的计算,为高频考点,把握元素化合价的变化、电子守恒为解答的关键,侧重分析与计算能力的考查,注意选项D中碘酸根离子被还原生成碘单质为本题的易错点,题目难度不大.

练习册系列答案
相关题目
15.根据有机化合物的系统命名原则,下列烃的命名正确的是( )
| A. | 2-乙基戊烷 | B. | 2-甲基-1-乙基苯 | ||
| C. | 2,4,4-三甲基己烷 | D. | 3-甲基-2-丁烯 |
16.炒菜的时候,加入少量的酒和醋,可使菜变得香醇可口,原因是( )
| A. | 有盐类物质产生 | B. | 有酸类物质产生 | C. | 有糖类物质产生 | D. | 有酯类物质产生 |
13.下列说法不正确的是( )
| A. | 蛋白质在酶或酸、碱的作用下能发生水解,最终生成氨基酸 | |
| B. | 人体的主要供能物质:葡萄糖、脂肪、蛋白质中,脂肪的供能最高 | |
| C. | 某些具有酸味的含有丰富维生素C的新鲜水果、蔬菜,是酸性食物 | |
| D. | 洁净的自来水是人体每天补充水分的最好选择 |
20.下列说法不正确的是( )
| A. | 铁在潮湿的空气中易发生吸氧腐蚀生成Fe(OH)2,进一步被O2氧化为Fe(OH)3,Fe(OH)3脱去一部分水生成Fe2O3•nH2O,它就是铁锈的主要成分 | |
| B. | 分子筛中有许多笼状空穴和通道可用于分离、提纯气体,还可用作干燥剂、离子交换剂、催化剂和、催化剂载体 | |
| C. | 俄国化学家门捷列夫经过研究提出了元素周期律--元素性质随着元素原子量(相对原子质量)递增而呈周期性变化的规律,并列出第一张元素周期表 | |
| D. | 氧化铝陶瓷、硅藻土、沸石、立方氮化硼都是无机非金属材料,光导纤维、聚酯纤维、橡胶、酚醛树脂都是高分子材料 |
14.已知正四面体形分子E和直线型分子F反应,生成四面体形分子L和直线型分子M.(组成E分子的元素的原子序数小于10,组成F分子的元素为第三周期的元素.)如图,则下列判断中正确的是 ( )
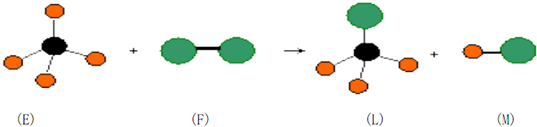

| A. | 常温常压下,L是一种液态有机物 | B. | E中化学键是极性键 | ||
| C. | F具有漂白性 | D. | 上述反应的类型是取代反应 |
 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$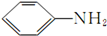 (有弱碱性,易被氧化).
(有弱碱性,易被氧化).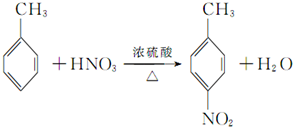 ,该反应要控制好低温条件,否则会生成一种新物质F,该物质是一种烈性炸药,F的名称为2,4,6-三硝基甲苯.
,该反应要控制好低温条件,否则会生成一种新物质F,该物质是一种烈性炸药,F的名称为2,4,6-三硝基甲苯.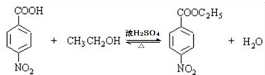 .
.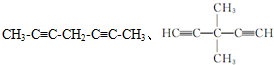 .
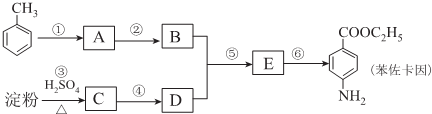
.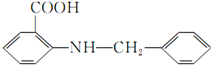 是一种药物中间体,请写出以甲苯为主要原料制备该中间体的合成路线流程图:
是一种药物中间体,请写出以甲苯为主要原料制备该中间体的合成路线流程图: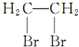
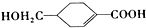 的合成路线(部分反应条件略去)如图所示:
的合成路线(部分反应条件略去)如图所示: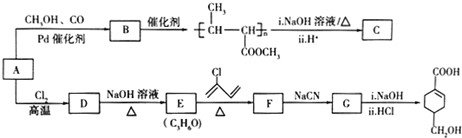
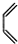 +
+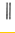 $\stackrel{△}{→}$
$\stackrel{△}{→}$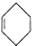 ,R-C≡N$→_{ii.HCl}^{i.NaOH}$R-COOH,
,R-C≡N$→_{ii.HCl}^{i.NaOH}$R-COOH,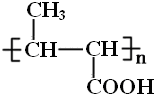 ,D→E的反应类型为取代反应或水解反应;
,D→E的反应类型为取代反应或水解反应;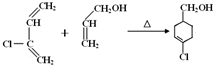 ;
;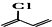 中最多有10个原子共平面,
中最多有10个原子共平面,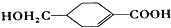 发生缩聚反应生成有机物的结构简式为
发生缩聚反应生成有机物的结构简式为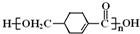 ;
;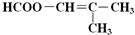 (写结构简式).
(写结构简式).