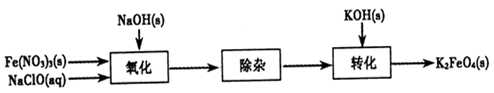
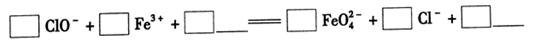��Ŀ����
��Ҫ����ա�
(1)��S2����Fe2����Fe3����Mg2����S��I����H���У�ֻ�������Ե��� ��ֻ�л�ԭ�Ե��� ���������������л�ԭ�Ե��� ��
(2)ijͬѧд������������ѧ����ʽ(δ��ƽ)
��NO��HNO3�D��N2O3��H2O
��NH3��NO�D��HNO2��H2O
��N2O4��H2O�D��HNO3��HNO2
��������Ϊһ��������ʵ�ֵ��� ��
(3)��������������ԭ��Ӧ�У���������ǿ�������� ��
��2FeCl3��2KI=2FeCl2��2KCl��I2
��2FeCl2��Cl2=2FeCl3
��2KMnO4��16HCl(Ũ)=2KCl��2MnCl2��5Cl2����8H2O
��������Cl����I�����棬Ϊ������I����Cl�������������������⣬��Ӧ��������Ӧ�е� ����������
(1)Fe3����Mg2����H����I����S2����Fe2����S��(2)��
(3)KMnO4��FeCl3
����

��ϰ��ϵ�д�
 ���������������Բ��������ϵ�д�
���������������Բ��������ϵ�д�
�����Ŀ
��֪Br2+ 2Fe2+ = 2Fe3++ 2 Br-������1 molFeBr2��Һ����ͨ��Cl2����Һ����һ���Br-����ʱ�������жϲ���ȷ����
| A����Ӧǰ����Һ����ɫ�����˸ı� |
| B����Ӧ����Һ��c(Cl-)= C(Br-) |
| C���μӷ�Ӧ��Cl2Ϊ1 mol |
| D����Ӧ�����ӷ���ʽΪ��2Fe2++ 2Br- + 2Cl2= 2Fe3++ Br2 + 4Cl- |
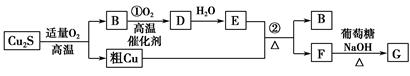
 (NxOy)�� H2O(��ƽʱx��y�þ�����ֵ��ʾ����������
(NxOy)�� H2O(��ƽʱx��y�þ�����ֵ��ʾ���������� CO(NH2)2 (l��+ H2O (l)��
CO(NH2)2 (l��+ H2O (l)��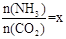 ����ͼ�ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ��������x����������ԭ���� ��
����ͼ�ǰ�̼�ȣ�x����CO2ƽ��ת���ʣ������Ĺ�ϵ��������x����������ԭ���� ��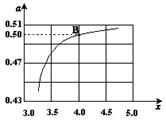
 7N2��12 H2OҲ�ɴ���NO2����ת��1.2 mol����ʱ�����ĵ�NO2�ڱ�״������ L��
7N2��12 H2OҲ�ɴ���NO2����ת��1.2 mol����ʱ�����ĵ�NO2�ڱ�״������ L�� 2SO3��g�� ��H="-196.6" kJ��mol-1
2SO3��g�� ��H="-196.6" kJ��mol-1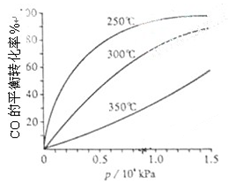
 Fe(OH)3��5OH��]
Fe(OH)3��5OH��]