题目内容
2.下列关于价层电子对互斥理论及杂化轨道理论的叙述不正确的是( )| A. | 价层电子对互斥理论将分子分成两类:中心原子有孤电子对的和无孤电子对的 | |
| B. | 价层电子对互斥理论既适用于单质分子,也适用于化合物分子 | |
| C. | sp3杂化轨道是由一个原子中能量相近的s轨道和p轨道通过杂化形成的一组能量相近的新轨道 | |
| D. | AB2型共价化合物的中心原子A采取的杂化方式可能不同 |
分析 A.中心原子的最外层电子有的全部成键,有的部分成键;
B.价层电子对互斥理论只适用于化合物分子;
C.sp3杂化轨道是由同一个原子中能量最近的s轨道和p轨道混合起来形成的一组能量相同的新轨道,杂化后的各轨道完全相同;
D.AB2型共价化合物的中心原子的价层电子对数不一定相同.
解答 解:A.中心原子的最外层电子有的全部成键,有的部分成键,全部成键的原子中没有孤电子对,部分成键的原子含有孤电子对,所以价层电子对互斥理论将分子分成两类:中心原子有孤电子对的和无孤电子对的,故A正确;
B.价层电子对互斥理论只适用于化合物分子,单质分子中不存在中心原子,不能用价层电子对互斥理论解释,故B错误;
C.sp3杂化轨道是由同一个原子中能量最近的s轨道和p轨道混合起来形成的一组能量相同的新轨道,杂化后的各轨道完全相同,故C正确;
D.AB2型共价化合物的中心原子的价层电子对数不一定相同,如CO2为sp杂化,SO2为sp2杂化,故D正确.
故选B.
点评 本题考查了价层电子对互斥理论的用途,明确价层电子对互斥理论原理是解本题关键,题目难度中等,侧重于考查学生对基本原理的应用能力.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
13.我国首部《食品安全法》于2009年6月1日起颁布施行.下列能保证食品安全的是( )
| A. | 用小苏打作发酵粉焙制糕点 | B. | 用甲醛溶液浸泡海产品 | ||
| C. | 用工业石蜡给水果上蜡“美容” | D. | 用工业酒精勾兑饮用酒 |
10.O2F2可以发生反应:H2S+O2F2→SF6+HF+O2(未配平).下列说法正确的是( )
| A. | O2是还原产物 | |
| B. | O2F2中氧分子与氟分子比例为1:l | |
| C. | 每生成2.24LHF,转移0.4mol电子 | |
| D. | 氧化剂与还原剂的物质的量之比为l:4 |
7.现有a L乙烷、乙烯和氢气的混合气体,在一定条件下充分反应得到b L气体(温度、压强相同),将反应后气体通入酸性高锰酸钾溶液中,气体体积不变.则原气体中乙烯的体积分数为( )
| A. | $\frac{a}{a+b}$ | B. | $\frac{a-b}{a+b}$ | C. | $\frac{a-b}{a}$ | D. | $\frac{a+b}{a}$ |
6.中美科学家研制的某快充电池工作原理如图所示.电解质为一种常温离子液体(由有机阳离子、Al2Cl7-和AlCl4-组成),在电池充、放电过程中,不产生其他离子且有机阳离子不参与电极反应.下列有关该快充电池的说法错误的是( )
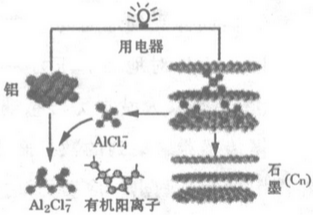

| A. | 放电时铝为电池阳极 | |
| B. | 充电时AlCl4-移向石墨电极 | |
| C. | 铝电极的比能量较高 | |
| D. | 充电时铝电极上的反应为Al+7AlCl4--3e-=4Al2Cl7- |

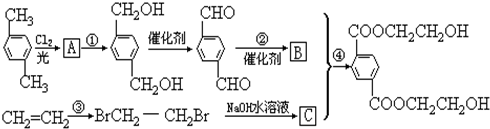
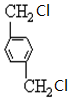 、
、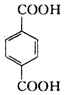 、HOCH2CH2OH.
、HOCH2CH2OH.