题目内容
7.下列短周期元素的原子序数大小顺序为C>A>B>D>E,A、C同周期,B、C同主族.A与B形成离子化合物A2B,A2B中所有离子的电子数相同,其电子总数为30;D和E可形成4核10个电子分子.试回答下列问题:(1)写出五种元素的元素符号:ANa、BO、CS、DN、EH.
(2)用电子式表示离子化合物A2B的形成过程:
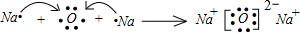 .
.(3)同时含有A、B、C、E四种元素的两种常见化合物之间可以发生化学反应,那发生反应的离子方程式为HSO3-+H+=H2O+SO2↑.
(4)D单质的结构式为N≡N.
(5)A、B两元素组成的化合物A2B2属于离子(填离子或共价)化合物,存在的化学键是离子键和共价键键.
分析 A与B形成离子化合物A2B,A2B中所有离子的电子数相同,且电子总数为30,所以每个离子都有10个电子,由化学式的结构可知,B带2个单位负电荷,A带1个单位正电荷,所以A是Na元素,B是O元素,因为A、C同周期,B与C同主族,所以C为S元素;D和E可形成4核10电子的分子,每个原子平均不到3个电子,可知其中一定含有氢原子,分子中有4个原子核共10个电子,一定是NH3,结合原子序数D>E,可知D是N元素,E是H元素,据此解答.
解答 解:A与B形成离子化合物A2B,A2B中所有离子的电子数相同,且电子总数为30,所以每个离子都有10个电子,由化学式的结构可知,B带2个单位负电荷,A带1个单位正电荷,所以A是Na元素,B是O元素,因为A、C同周期,B与C同主族,所以C为S元素;D和E可形成4核10电子的分子,每个原子平均不到3个电子,可知其中一定含有氢原子,分子中有4个原子核共10个电子,一定是NH3,结合原子序数D>E,可知D是N元素,E是H元素,
(1)由上述分析可知,A为Na,B为O,C为S,D为N,E为H,
故答案为:Na;O;S;N;H;
(2)A2B是Na2O,由钠离子与氧离子形成的离子化合物,Na2O的形成过程为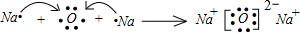 ,
,
故答案为: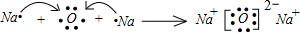 ;
;
(3)同时含有A、B、C、E四种元素的两种常见化合物为NaHSO4和NaHSO3,两者的反应实际上是HSO3-与H+的反应:HSO3-+H+=H2O+SO2↑,故答案为:HSO3-+H+=H2O+SO2↑;
(4)D为氮元素,单质中氮原子之间形成3对共用电子对,结构式为N≡N.
故答案为:N≡N.
(4)A、B两元素组成的化合物A2B2即为Na2O2,为离子化合物,结构中钠离子和过氧根之间为离子键,过氧根中为共价键,故答案为:离子,离子键和共价键.
点评 以元素推断为载体,考查结构位置关系、电子式等化学用语、晶体类型与化学键,难度不大,推断元素是解题关键,注意基础知识的掌握与运用,是对学生能力的综合考查.

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案| A. | 0.225 | B. | 0.30 | C. | 0.36 | D. | 0.45 |
| A. | Na2O2投入水中:2Na2O2+2H2O=4Na++4OH-+H2↑ | |
| B. | 向次氯酸钠溶液中通入足量SO2气体:ClO-+SO2+H2O=HClO+HSO3- | |
| C. | 钠投入CuSO4溶液中:2Na+Cu2++2H2O=2Na++Cu(OH)2↓+H2↑ | |
| D. | 铜和稀HNO3反应:3Cu+8H++2NO3-=3Cu2++2NO2↑+4H2O |
 金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如图.下列有关绿原酸的说法中不正确的是( )
金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如图.下列有关绿原酸的说法中不正确的是( )| A. | 绿原酸分子中有1个手性碳原子 | |
| B. | 绿原酸分子中所有碳原子都能在同一平面上 | |
| C. | 绿原酸能发生显色反应、取代反应和加成反应 | |
| D. | 每摩尔绿原酸最多与含4molNaOH的溶液反应 |
| 选项 | 实验操作 | 预期现象 |
| A | 向AlCl3溶液中滴入过量的氨水 | 先有白色沉淀,后沉淀消失 |
| B | 向AgCl浊液中滴入KI溶液,振荡 | 白色浑浊逐渐转化为黑色沉淀 |
| C | 向Ca(ClO)2溶液中通入CO2,再滴入少量品红溶液 | 出现浑浊,滴入的品红变无色 |
| D | 向BaCl2溶液中先通入SO2,再通入NO2 | 先有白色沉淀,后沉淀消失 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 明矾净水:Al3++3H2O═Al(OH)3↓+3H+ | |
| B. | 硫酸镁与氢氧化钡溶液混合:SO${\;}_{4}^{2-}$+Ba2+═BaSO4↓ | |
| C. | 磷酸二氢钙与足量烧碱溶液反应:3Ca2++2H2PO${\;}_{4}^{-}$+4OH-═Ca3(PO4)2↓+4H2O | |
| D. | 氨水中通入过量的二氧化硫气体:NH3•H2O+SO2═NH${\;}_{4}^{+}$+HSO${\;}_{3}^{-}$ |
| A. | 若a:b=9:1,则R的化学式为FeO | |
| B. | 若a:b=1:10,则R的化学式为Fe2O3 | |
| C. | 若a:b=29:30,则R的化学式为Fe3O4 | |
| D. | 试验过程中被还原的Cl2为(10b-a)/8mol |