题目内容
17.在100mL HNO3和H2SO4混合溶液中,两种酸物质的量浓度之和0.6mol/L,向该溶液中加入足量铜粉,加热,待充分反应后,所得溶液中Cu2+物质的量浓度(mol/L)最大值为( )| A. | 0.225 | B. | 0.30 | C. | 0.36 | D. | 0.45 |
分析 发生反应离子方程式为:3Cu+2NO3-+8H+=3Cu2++2NO(g)+4H2O,由上述反应方程式可知,NO3-和H+的物质的量之比为1:4,氢离子与硝酸根恰好反应,生成的铜离子物质的量最大;设HNO3、H2SO4各为x、ymol,则n(NO3-):n(H+)=x:(x+2y)=1:4,x+y=0.6×0.1,据此计算x、y的值,再根据方程式计算铜离子的物质的量,根据c=$\frac{n}{V}$计算铜离子浓度.
解答 解:反应的离子方程式为:3Cu+2NO3-+8H+=3Cu2++2NO(g)+4H2O,铜足量,由上述反应方程式可知,NO3-和H+的物质的量之比为1:4,氢离子与硝酸根恰好反应,生成的铜离子物质的量最大,
设HNO3、H2SO4各为x、ymol,则n(NO3-):n(H+)=x:(x+2y)=1:4、x+y=0.6×0.1,
联立解得:x=0.024mol、y=0.036mol,
由方程式可知,生成铜离子的物质的量为:0.024mol×$\frac{3}{2}$=0.036mol,
所以铜离子的最大浓度为:$\frac{0.036mol}{0.1L}$=0.36mol/L,
故选C.
点评 本题考查化合物的有关计算,题目难度中等,确定NO3-和H+的物质的量之比为1:4时生成的铜离子浓度最大是解题的关键,注意利用离子方程式进行解答.

练习册系列答案
相关题目
7.乙醚极易挥发、微溶于水、是良好的有机溶剂.乙醇与浓硫酸的混合物在不同温度下反应能生成乙烯或乙醚.某实验小组用下图装置制取乙醚和乙烯.

有关物质沸点数据
(1)制乙醚:在蒸馏烧瓶中先加入10mL乙醇,慢慢加入10mL浓硫酸,冷却,固定装置.加热到140℃时,打开分液漏斗活塞,继续滴加10mL乙醇,并保持140℃,此时烧瓶c中收集到无色液体.
①Ⅰ和Ⅱ是反应发生装置,应该选择Ⅰ(选答“Ⅰ”或“Ⅱ”)与装置Ⅲ相连.
②乙醇通过分液漏斗下端连接的长导管插入到液面下加入,目的有二,一是使反应物充分混合,二是防止乙醇挥发.
③Ⅲ中水冷凝管的进水口是b(选答“a”或“b”).冰盐水的作用是凝液化乙醚.
④有同学认为以上装置还不够完善,一是溴水可能倒吸,二是尾气弥漫在空气中遇明火危险.该同学设计了以下几种装置与导管d连接,你认为合理的是(选填编号)c、d.
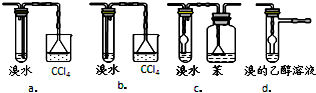
⑤反应一段时间后,升温到170℃,观察到反应物变为黑色,溴水褪色.写出实验过程中有气体生成的化学方程式(写两个方程式)CH3CH2OH+6H2SO4$\stackrel{△}{→}$2CO2↑+6SO2↑+↑+2H2O;C+2H2SO4$\stackrel{△}{→}$CO2↑+2SO2↑+2H2O、CH3CH2OH$→_{170℃}^{浓硫酸}$C2H4↑+H2O、CH3CH2OH+2H2SO4$\stackrel{△}{→}$2C+2SO2↑+5H2O(其中两个).
⑥实验中收集到的乙醚产品中可能含有多种杂质.某同学设计了以下提纯方案:
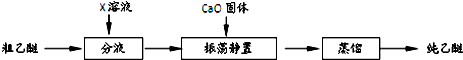
(2)分液步骤除去产品中的酸性杂质,则X可以是NaOH.
(3)蒸馏操作可除去的杂质是乙醇(CH3CH2OH).

有关物质沸点数据
| 物质 | 沸点 |
| 乙醚 | 34.6℃ |
| 乙醇 | 78.2℃ |
①Ⅰ和Ⅱ是反应发生装置,应该选择Ⅰ(选答“Ⅰ”或“Ⅱ”)与装置Ⅲ相连.
②乙醇通过分液漏斗下端连接的长导管插入到液面下加入,目的有二,一是使反应物充分混合,二是防止乙醇挥发.
③Ⅲ中水冷凝管的进水口是b(选答“a”或“b”).冰盐水的作用是凝液化乙醚.
④有同学认为以上装置还不够完善,一是溴水可能倒吸,二是尾气弥漫在空气中遇明火危险.该同学设计了以下几种装置与导管d连接,你认为合理的是(选填编号)c、d.

⑤反应一段时间后,升温到170℃,观察到反应物变为黑色,溴水褪色.写出实验过程中有气体生成的化学方程式(写两个方程式)CH3CH2OH+6H2SO4$\stackrel{△}{→}$2CO2↑+6SO2↑+↑+2H2O;C+2H2SO4$\stackrel{△}{→}$CO2↑+2SO2↑+2H2O、CH3CH2OH$→_{170℃}^{浓硫酸}$C2H4↑+H2O、CH3CH2OH+2H2SO4$\stackrel{△}{→}$2C+2SO2↑+5H2O(其中两个).
⑥实验中收集到的乙醚产品中可能含有多种杂质.某同学设计了以下提纯方案:

(2)分液步骤除去产品中的酸性杂质,则X可以是NaOH.
(3)蒸馏操作可除去的杂质是乙醇(CH3CH2OH).
8.空气污染已成为人类社会面临的重大威胁.下列气体中,不会造成空气污染的是( )
| A. | O2 | B. | SO2 | C. | Cl2 | D. | NO2 |
5.氢化氨(NH4H)与氯化铵(NH4Cl)结构相似.但NH4H与水反应有氢气生成,下列叙述正确的是( )
| A. | NH4H与水反应时,NH4H是还原剂 | B. | NH4H溶于水时,溶液显酸性 | ||
| C. | H-的离子半径小于Li+的离子半径 | D. | NH4H中只有离子键没有共价键 |
12.如图是一个化学反应的微观示意图,从示意图获取的信息正确的是( )
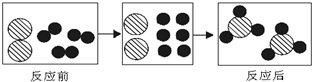

| A. | 反应前后分子种类不发生改变 | |
| B. | 反应前后原子的种类与数目发生改变 | |
| C. | 反应前两种分子的个数比是1:2 | |
| D. | 该反应的基本类型是化合反应 |
2.环境监测中心在公布城市空气质量报告时,不需要公布指标的项目是( )
| A. | 二氧化碳 | B. | 二氧化硫 | C. | 氮氧化物 | D. | 可吸入颗粒物 |
9.下列说法中不正确的是( )
| A. | 在燃煤中加入石灰石可减少SO2排放,发生的反应为:2CaCO3=2SO2+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CO2+2CaSO4 | |
| B. | C02通入水玻璃可以得到硅酸沉淀 | |
| C. | 硅主要以单质、氧化物、硅酸盐的形式存在于自然界中 | |
| D. | 氢氟酸能够雕刻玻璃,故不能用玻璃瓶来盛装氢氟酸 |
6.下列处理事故的方法正确的是( )
| A. | 将CO中毒者移至通风处抢救 | |
| B. | 误食硫酸铜溶液,可服用氢氧化钠溶液解毒 | |
| C. | 浓H2SO4溅到皮肤上,立即用碳酸钠稀溶液洗涤 | |
| D. | 氢氧化钠浓溶液溅入眼中,应立即用大量水冲洗,再用稀盐酸冲洗 |
 .
.